题目内容
【题目】A、B、C三种固体物质的溶解度曲线如图所示。请回答下列问题。
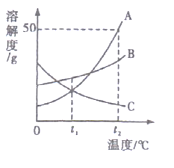
(1)t1℃时,A、B、C三种物质的饱和溶液中,溶质质量分数相等的是________。
(2)t2℃时,将75g A的饱和溶液与25g水混合,所得溶液中溶质的质量分数为________。
(3)将t2℃时等质量的A、B、C三种物质的饱和溶液,分别降温至t1℃时,所得溶液中溶剂质量由大到小的顺序为____________。
【答案】A和C 25% C>B>A
【解析】
(1)根据溶解度曲线可知,t1℃时,A、B、C三种物质的溶解度大小顺序为B>A=C,一定温度下饱和溶液的溶质质量分数=![]() ,A、B、C三种物质的饱和溶液中,溶质质量分数相等的是A和C;
,A、B、C三种物质的饱和溶液中,溶质质量分数相等的是A和C;
(2)t2℃时,A的溶解度为50g,根据溶解度概念可知,t2℃时,150g的饱和溶液中含有50gA,则75g A的饱和溶液中含有50g的水和25gA,将75g A的饱和溶液与25g水混合,所得溶液中溶质的质量分数=![]() ;
;
(3)t2℃时,A物质的溶解度最大,C物质的溶解度最小,等质量的A、B、C三种物质的饱和溶液中,A中的溶剂最少,C中的溶剂最多,所以将t2℃时等质量的A、B、C三种物质的饱和溶液,降温至t1℃时,溶剂质量不变,所得溶液中溶剂质量由大到小顺序为C>B>A。

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案【题目】“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的舞台。大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒中的乙醇生成乙酸乙酯。下表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为 _______;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为_______(计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X的化学式为________。