题目内容
【题目】如下表:原子结构是通过科学家不断地建立与修正原子结构模型,不断地实验,不断地思考研究而得到的.下表是原子结构模型的几种学说
时间 | 模型类型 | 科学家 | 内容 |
| 道尔顿模型 | 道尔顿(英国) | 原子是一个坚硬的小球 |
| 汤姆生模型 | 汤姆生(英国) | 发现电子,即“西瓜模型”正电荷是西瓜肉,电子是西瓜籽 |
| 卢瑟福模型 | 卢瑟福(英国) | 发现原子核,原子大部分体积是空的,电子围绕带正电的原子核随意动转 |
| 分层模型 | 玻尔(丹麦) | 电子在固定轨道上分层运动(绕着原子核) |
现代 | 电子云模型 | 电子出现在原子核周围,有的区域次数多,有的区域次数少 |
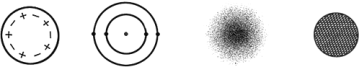
![]() 上面四种原子结构模型中道尔顿的原子结构模式是________(填序号),这种原子模型是一种________结构.
上面四种原子结构模型中道尔顿的原子结构模式是________(填序号),这种原子模型是一种________结构.
![]() 年,______通过实验发现原子结构,所做的实验名称是________,实验中大多数
年,______通过实验发现原子结构,所做的实验名称是________,实验中大多数![]() 微粒不改变原来的运动方向,顺利通过.有一小部分
微粒不改变原来的运动方向,顺利通过.有一小部分![]() 微粒发生了偏转,原因是________;极少数
微粒发生了偏转,原因是________;极少数![]() 微粒被反弹了回来,原因是________.因此,卢瑟福根据实验建立了________原子模型.
微粒被反弹了回来,原因是________.因此,卢瑟福根据实验建立了________原子模型.
![]() 请用框图的形式表示原子的结构:
请用框图的形式表示原子的结构:
【答案】④实心卢瑟福实验(或![]() 粒子散射实验)原子核带正电,
粒子散射实验)原子核带正电,![]() 粒子带正电,当
粒子带正电,当![]() 粒子靠近原子核时受到原子核的斥力极少数的
粒子靠近原子核时受到原子核的斥力极少数的![]() 粒子撞击到原子核,原子核质量远远大于
粒子撞击到原子核,原子核质量远远大于![]() 粒子核式核式
粒子核式核式
【解析】
(1)道尔顿说原子是一个坚硬的小球,是图中的第四个选项,由图可知,这种结构是一个实心的结构;
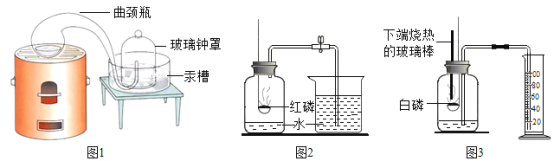
(2)1911年著名物理学家卢瑟福等人做了一个著名的“卢瑟福实验”(或α粒子散射实验):用一束带正电的质量比电子大很多的高速运动的α粒子轰击金箔,结果是大多数α粒子能穿过金箔且不改变原来的前进方向,但也有一小部分改变了原来的方向,甚至有极少数的α粒子被反弹了回来。有极少数的α粒子被反弹了回来,说明遇到了质量很大的东西,即原子核质量很大,且带正电荷;大多数α粒子能穿过金箔且不改变原来的前进方向,说明原子核的体积很小,原子核外空间很大;一小部分改变了原来的方向,又因为原子核带正电,α粒子带正电,所以遇到了带正电的微粒才改变了方向。卢瑟福根据α粒子散射实验建立了原子的核式结构模型。
(3)原子是由原子核和核外电子构成的,原子核带正电,核外电子带负电,而原子核又是由质子和中子构成的,质子带正电,中子不带电, 。
。

 孟建平名校考卷系列答案
孟建平名校考卷系列答案【题目】化学小组的同学在做镁条在空气中燃烧实验时,发现生成的白色固体中还夹杂着少量的淡黄色的固体。(提出问题)为什么会生成淡黄色固体?(查阅资料)记录了下列几种物质的颜色:
物质 | MgO(氧化镁) | MgCl2 | Mg3N2 (氮化镁) | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
小红同学认为不必查阅氯化镁的颜色,理由是:___________________。
(提出猜想)分析资料小红认为淡黄色固体可能是和空气中的_____________反应生成的。
(实验探究)小红设计实验来验证自己的猜想,他的方案可能是:__________。
(实验结论)根据小红的实验结果,写出镁条在空气中燃烧的两个符号表达式①_____________; ②____________________________。
(反思与评价)通过上述实验,你对燃烧有什么新认识________________