题目内容
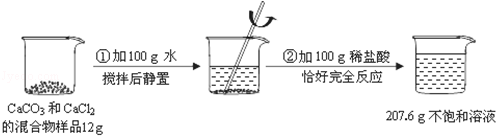
将12g的石灰石放入烧杯中,加入一定量的稀盐酸,待恰好完全反应后,测得产生4.4g气体(杂质不溶于水,也不参加反应)。
计算:该石灰石中钙元素的质量分数是多少?(结果保留整数)
解:设石灰石中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g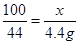
x=10g
该石灰石中钙元素的质量=10g×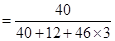 ×100%=4g
×100%=4g
该石灰石中钙元素的质量分数=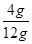 ×100%=33%
×100%=33%
答:该石灰石中钙元素的质量分数是33%。
解析试题分析:首先根据碳酸钙与稀盐酸反应的化学方程式及生成二氧化碳的质量计算出石灰石中碳酸钙的质量,然后根据碳酸钙中钙元素的质量分数及碳酸钙的质量计算出样品中钙元素的质量,最后再结合样品和钙元素的质量计算出该石灰石样品中钙元素的质量分数。
考点:根据化学方程式的计算,根据化学式的计算。

练习册系列答案
相关题目
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,将四份不同质量的样品加入到四份稀盐酸中,进行实验,结果如下:
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.54 | 3.08 | 4.4 | m |
(1)上表中m的数值是__________________;
(2)试计算这种石灰石矿中碳酸钙的质量分数。
(3)第三次反应后所得溶液的溶质质量分数是多少?
为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,贝贝同学取10g黄铜样品放入烧杯中,再取40g稀盐酸分四次加入烧杯中,均充分反应,实验数据如下:
| | 第一次 | 第二次 | 第二次 | 第四次 |
| 加入稀盐酸质量(g) | 10g | 10g | 10g | 10g |
| 剩余固体的质量(g) | 8.7g | 7.4g | 6.1g | 5.45g |
(1)该小组同学要用质量分数为36,5%浓盐酸配制所需的40克稀盐,则需浓盐酸的质量为_ ;
(2)上述反应的化学方程式为 ;
(3)列出求解生成氢气总质量(X)的比例式 ;
(4)向第一次反应后所得溶液中加入8.74g水,则所得溶液的质量分数为 ;
(5)某工厂要想制得2000t黄铜,需要含杂质50%的辉铜矿(主要成分是Cu2S)的质量为 .