题目内容
【题目】2018年4月美国对中国企业中兴通讯禁售手机芯片等,芯片的制造引起了热议,而制造芯片的主要原材料是高纯硅。高纯硅制备方法之一的工业流程如下:
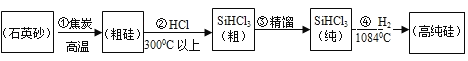
资料:SiHCl3能与H2O剧烈反应;在空气中易自燃;粗SiHCl3(沸点33.0℃)中含有少量SiCl4(沸点57.6℃)和HCl(沸点﹣84.7℃)
(1)流程①中利用了焦炭的_____性。流程③中的精馏温度应不超过_____。
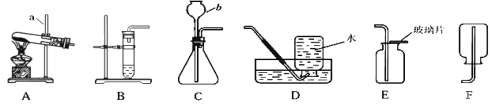
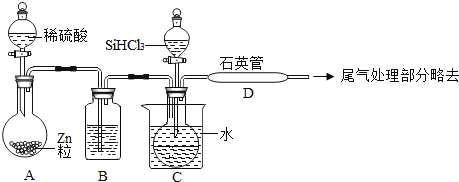
(2)流程④制备高纯硅的装置如图(热源及夹持装置略去):
①流程④的化学反应为置换反应,写出其化学方程式:_____。
②装置B中的试剂是_____;装置C中的烧瓶需要加热,其目的是_____。
③反应一段时间后,装置D中观察到的现象是_____。
④为保证制备高纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及_____。
(3)该流程中能够循环利用的物质是_____。
【答案】还原 33℃ SiHCl3+H2![]() Si+3HCl 浓硫酸 使进入烧瓶的液态SiHCl3变为气体 有固体物质生成 排尽装置内的空气 HCl。
Si+3HCl 浓硫酸 使进入烧瓶的液态SiHCl3变为气体 有固体物质生成 排尽装置内的空气 HCl。
【解析】
二氧化硅和碳在高温的条件下生成硅和一氧化碳,SiHCl3和氢气在高温的条件下生成硅和氯化氢,硅极易被氧化生成氧化硅。
(1)二氧化硅和碳在高温的条件下生成硅和一氧化碳,粗SiHCl3(沸点33.0℃),所以流程①中利用了焦炭的还原性,流程③中的精馏温度应不超过33℃。
(2)①SiHCl3和氢气在高温的条件下生成硅和氯化氢,化学方程式为
SiHCl3+H2![]() Si+3HCl。
Si+3HCl。
②SiHCl3能与H2O剧烈反应,在空气中易自燃,浓硫酸具有吸水性,所以装置B中的试剂是浓硫酸,装置C中的烧瓶需要加热,其目的是:使进入烧瓶的液态SiHCl3变为气体。
③SiHCl3和氢气在高温的条件下生成硅和氯化氢,所以反应一段时间后,装置D中观察到的现象是:有固体物质生成。
④硅极易被氧化,所以为保证制备高纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及排尽装置内的空气。
(4)既是反应物,也是生成物的物质可以循环利用,所以该流程中能够循环利用的物质是HCl。