题目内容
【题目】I、用所学化学知识填空。
(1)下列材料不属于合金的是____(填“陶瓷”或“硬铝”)。
(2)改良酸性土壤可以用____(填“烧碱”或“消石灰”);
(3)打开瓶塞,在空气中能产生“白雾”的是____(填“浓硫酸”或“浓盐酸”);
(4)用井水洗衣服时,肥皂不易起泡沫且产生浮渣,该井水是____(填“硬水”或“软水”)。
II、请完善网络图,并根据图示关系回答下列问题:
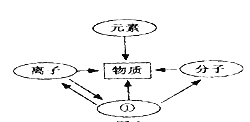
(1)物质是由 __________组成的;
(2)构成物质的微粒有分子、离子和 ______________;
(3)分子是由 ________________构成的;
(4)原子得到电子转化为________________(填“阳离子”或“阴离子”)。
【答案】 陶瓷 石灰 浓盐酸 硬水 元素 原子 原子 阴离子
【解析】根据所学知识知,I、(1)不属于合金的是陶瓷,硬铝属于铝合金。(2)改良酸性土壤可以用消石灰,价格便宜。(3)打开瓶塞,在空气中能产生“白雾”的是浓盐酸,浓盐酸具有挥发性,易形成白雾。(4)用井水洗衣服时,肥皂不易起泡沫且产生浮渣,该井水是硬水,硬水泡沫少。II、根据所学知识和题中信息知,(1)物质是由元素组成的,元素属于宏观概念;(2)构成物质的微粒有分子、离子和原子,分子、离子和原子都是构成物质的一种微粒;(3)分子是由原子构成的;(4)原子得到电子转化为阴离子,核内质子数小于核外电子数。
点睛∶改良酸性土壤常用消石灰。肥皂水遇硬水,泡沫少,遇软水,泡沫多。分子、离子和原子都是构成物质的一种微粒。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】小明取酸性锌锰干电池进行探究,他发现电池内部结构如图1所示。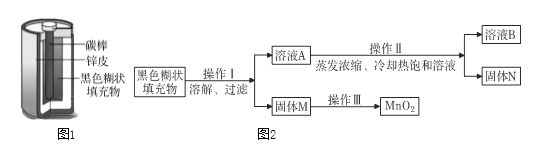
【查阅资料】(1)锌皮为金属锌(含有少量的铁)
(2)黑色糊状填充物由炭黑、MnO2、ZnC12和NH4Cl等组成
(3)有关数据见下表
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 | |
【实验探究一】小明取适量黑色糊状填充物,按图2所示实验流程进行探究。
(1)溶液A中溶质主要有______(填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是____________。
(2)欲从固体M 中得到较纯的MnO2,操作Ⅲ可采用的简便方法是____________。
【实验探究二】小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
(1)取一块锌皮放入盛有适量稀盐酸的烧杯中,有ZnCl2生成。
① 实验中可观察到的现象是_________;
② 下列各组物质混合后,也能生成ZnCl2的有_________(填字母序号)。
A.ZnO与稀盐酸 B.ZnSO4溶液与BaC12溶液
C.ZnCO3与NaCl溶液 D.Zn(NO3)2溶液与NH4Cl溶液
(2)另取一块锌皮放入盛有一定量CuSO4溶液的烧杯中,充分反应后得到溶液E和固体F。当溶液E中只含一种溶质时,该溶质是________(填化学式);当固体F中只含一种物质时,溶液E中最少含有________种溶质。
③若将6.5g锌皮与足量稀硫酸完全反应,则生成氢气的质量________0.2g(选填“<”、“>”或“=”)。