题目内容
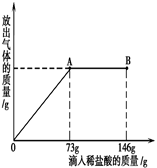
某厂生产的纯碱中含有少量氯化钠.取12g该样品于烧杯中,并滴加稀盐酸至73g时,气泡不再冒出,此时称得烧杯内溶液的总质量为80.6g.请计算:
(1)产生二氧化碳气体的质量是多少?
(2)样品中碳酸钠的质量;
(3)所得溶液中溶质的质量分数是多少(结果保留整数)
(1)产生二氧化碳气体的质量是多少?
(2)样品中碳酸钠的质量;
(3)所得溶液中溶质的质量分数是多少(结果保留整数)
(1)4.4g;(2)10.6g;(3)16%
试题分析:(1)12g+73g-80.6g=4.4g
(2)设 12g样品中Na2CO3的质量为X,反应生成的NaCl的质量为Y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
X Y 4.4g
106:X=117:Y=44:4.4g
X=10.6g Y=11.7g
则样品中Na2CO3的质量为10.6g。
(3)所得溶液中溶质的质量分数是
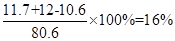
点评:这是化学反应联系方程式的计算题,这种题目是每年中考的压轴题,必考题,这类题目的难点在于理顺题目中的已知条件。

练习册系列答案
相关题目
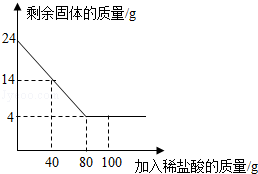
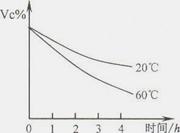
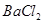 的固体混合物49.3g,加入167g蒸馏水,完全溶解后向该混合溶液中逐滴加入142g的
的固体混合物49.3g,加入167g蒸馏水,完全溶解后向该混合溶液中逐滴加入142g的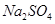 溶液,恰好反应生成
溶液,恰好反应生成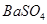 沉淀的质量为23.3g。(提示:BaCl2+Na2SO4=BaSO4↓+2NaCl)。计算恰好完全反应时所得溶液中溶质的质量分数是多少?
沉淀的质量为23.3g。(提示:BaCl2+Na2SO4=BaSO4↓+2NaCl)。计算恰好完全反应时所得溶液中溶质的质量分数是多少?