题目内容
称取NaCl和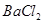 的固体混合物49.3g,加入167g蒸馏水,完全溶解后向该混合溶液中逐滴加入142g的
的固体混合物49.3g,加入167g蒸馏水,完全溶解后向该混合溶液中逐滴加入142g的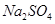 溶液,恰好反应生成
溶液,恰好反应生成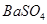 沉淀的质量为23.3g。(提示:BaCl2+Na2SO4=BaSO4↓+2NaCl)。计算恰好完全反应时所得溶液中溶质的质量分数是多少?
沉淀的质量为23.3g。(提示:BaCl2+Na2SO4=BaSO4↓+2NaCl)。计算恰好完全反应时所得溶液中溶质的质量分数是多少?
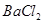 的固体混合物49.3g,加入167g蒸馏水,完全溶解后向该混合溶液中逐滴加入142g的
的固体混合物49.3g,加入167g蒸馏水,完全溶解后向该混合溶液中逐滴加入142g的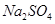 溶液,恰好反应生成
溶液,恰好反应生成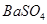 沉淀的质量为23.3g。(提示:BaCl2+Na2SO4=BaSO4↓+2NaCl)。计算恰好完全反应时所得溶液中溶质的质量分数是多少?
沉淀的质量为23.3g。(提示:BaCl2+Na2SO4=BaSO4↓+2NaCl)。计算恰好完全反应时所得溶液中溶质的质量分数是多少?12%
试题分析:解:设恰好反应后所得溶液中氯化钠的质量为x,参加反应氯化钡的质量为y
BaCl2+Na2SO4====BaSO4↓+2NaCl
208 233 117
y 23.3g x
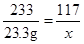
解得
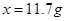

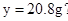
反应后生成氯化钠的总质量为
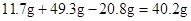
恰好反应后所得溶液中氯化钠的质量分数为
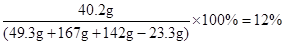
答:恰好完全反应时所得溶液中溶质的质量分数是12%
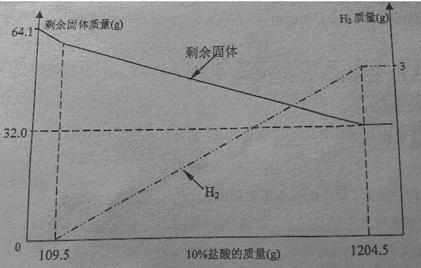
点评:这是化学反应联系方程式的计算题,这种题目是每年中考的压轴题,必考题,这类题目的难点在于把坐标曲线表示的意义和题干联系起来。

练习册系列答案
相关题目