题目内容
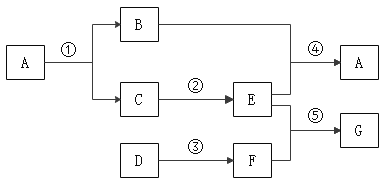
【题目】A~G均为初中化学常见物质,如图所示是它们之间的转化关系(部分反应物、生成物及反应条件已略去)。其中A是常用的补钙剂,D是黑色粉末,G是蓝色沉淀。请回答下列问题:
(1)B物质属于__________(选填“酸”“碱”“盐”或“氧化物”)
(2)写出实现转化③⑤的化学方程式:
转化③__________________;
转化⑤__________________。
(3)转化②属于____________(选填“放热”或“吸热”)反应。
(4)图中没有涉及到的基本反应类型为_________。
(5)F的水溶液中的阳离子是_________(填离子符号)。
【答案】氧化物 CuO+2HCl=CuCl2+H2O CuCl2+Ca(OH)2=Cu(OH)2↓+CaCl2 放热 置换反应 Cu2+
【解析】
A是常用的补钙剂,则A可能是碳酸钙,A能转化为B和C,C能转化为E,B与E转化为A,碳酸钙高温分解产生氧化钙和二氧化碳,氧化钙与水反应产生氢氧化钙,氧化碳与氢氧化钙溶液反应产生碳酸钙沉淀和水,所以B为二氧化碳,C为氧化钙,E为氢氧化钙;
D是黑色粉末,D可能是氧化铜,D能转化为F,E(氢氧化钙)与F能转化为G,G为蓝色沉淀,氧化铜与稀盐酸反应产生氯化铜和水,氯化铜与氢氧化钙反应产生蓝色沉淀氢氧化铜和氯化钙;所以F是氯化铜,G为氢氧化铜,代入框图验证,猜想正确。
根据以上分析可知:
(1)B物质是二氧化碳,二氧化碳只由碳、氧两种元素组成属于氧化物;
(2)转化③中:氧化铜与稀盐酸反应产生物质氯化铜溶液和水的化学方程式:CuO+2HCl=CuCl2+H2O;
转化⑤中:氯化铜与氢氧化钙反应产生氢氧化铜沉淀和氯化钙的化学方程式:CuCl2+Ca(OH)2=Cu(OH)2↓+CaCl2;
(3)转化②氧化钙与水反应产生物质氢氧化钙溶液,CaO+H2O=Ca(OH)2该反放出大量的热,属于放热反应。
(4)①碳酸钙受热分解属于分解反应;②氧化钙与水反应产生物质氢氧化钙溶液属于化合反应;③和⑤都属于复分解反应,图中没有涉及到的基本反应类型为:置换反应;
(5)F的水溶液为氯化铜溶液,阳离子是:铜离子(Cu2+);