题目内容
【题目】某同学在复习中和反应知识时思考,除了通过酚酞变色说明氧氧化钠与稀盐酸能发生反应,还有什么方法能说明两者发生了反应?同学们讨论后进行以下实验探究。
方案一:测定氢氧化钠和稀盐酸混合前后的pH。
(实验探究)甲组同学将一定量的稀盐酸加入pH=13的氢氧化钠溶液中,均匀混合后测定此时溶液的pH=5.
(得出结论)稀盐酸与氢氧化钠溶液发生了反应,并且该反应中__________过量,该反应的化学方程式为________________。
(交流讨论)乙组同学将一定量的稀盐酸加入 pH=13 的氢氧化钠溶液中,均匀混合后测定此时溶液的 pH=8.同学们认为该数据也能证明稀盐酸与氢氧化钠溶液发生了反应.你同意这种说法吗?__________(填“同意”或“不同意”),理由是_______________________。
方案二:小林同学将稀盐酸逐滴匀速加入一定量的稀氢氧化钠溶液中,用数字化仪器对反应过程中溶液的温度进行实时测定,得到的曲线如图1所示。
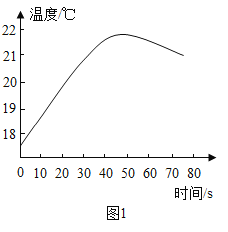
同学们认为根据该图象也能判断出稀盐酸与稀氢氧化钠溶液发生了反应,该反应是_______________ (填“放热”或“吸热”)反应,请你根据图中曲线判断大约____________秒时二者恰好完全反应。
(反思质疑)小涛同学通过测定氢氧化钠固体与稀盐酸混合前后的温度变化,证明两者发生了反应。小组同学一致认为该方案不合理,理由是______________。
(实验拓展)化学实验中还有很多物质反应没有明显的现象,如将二氧化碳通入氢氧化钠溶液中无明显现象.小组同学设计了如图2所示实验证明反应可以发生.实验过程中试管内液面上升,同学们认为该现象说明二者发生了反应,有同学认为该方案不严谨,理由是__________________,你的改进方法是___________,请你再设计出一种不同的实验方案证明氢氧化钠溶液与二氧化碳确实发生了化学反应:______________。

【答案】稀盐酸 NaOH+HCl= NaCl+H2O 不同意 加入稀盐酸时,氢氧化钠溶液被稀释,氢氧化钠溶液稀释时pH也减小 放热 50 氢氧化钠固体溶于水放热 二氧化碳能够溶于水 设计和图2相同的实验装置,把氢氧化钠溶液换成相同体积的水进行对比试验,观察液面上升高度 取混合后的溶液于试管中,加入足量稀盐酸,产生气泡,说明氢氧化钠和二氧化碳发生了反应.
【解析】
方案一:
得出结论:
稀盐酸与氢氧化钠溶液发生了反应生成氯化钠和水,完全反应后溶液pH小于7,并说明该反应中稀盐酸过量,该反应方程式为:NaOH+HCl= NaC1+H2O;
交流讨论:
不同意这种说法,理由是加入稀盐酸时,氢氧化钠溶液被稀释,氢氧化钠溶液稀释时pH也减小;
方案二:
过程中溶液的温度升高,说明该反应是放热反应,根据图中曲线判断大约50秒时,溶液的温度最高,二者恰好完全反应;
反思质疑:
该方案不合理,理由是氢氧化钠固体溶于水放热;
实验拓展:
该方案不严谨,理由是二氧化碳能够溶于水,改进方法是:设计和图2相同的实验装置,把氢氧化钠溶液换成相同体积的水进行对比试验,观察液面上升高度;氢氧化钠与二氧化碳反应生成碳酸钠和水,若能证明通入二氧化碳后溶液中存在碳酸钠即可说明二氧化碳能与碳酸钠反应,碳酸钠与盐酸反应生在氯化钠、水和二氧化碳。证明氢氧化钠溶液与二氧化碳确实发生了化学反应的实验方案:取混合后的溶液于试管中,加入足量稀盐酸,产生气泡,说明氢氧化钠和二氧化碳发生了反应。

【题目】(1)用稀盐酸和氢氧化钠溶液进行中和反应实验时,反应过程中溶液pH变化曲线如图所示:

①该反应的化学方程式是________________;
②该实验操作是将__________(写溶质的化学式)溶液逐滴加入到另一种溶液中。
(2)若用稀硫酸代替(1)中的稀盐酸,将稀硫酸逐滴加入至盛有氢氧化钠溶液的烧杯中,当滴加到一定量并充分反应时,请对烧杯中溶质成分进行探究。
(提出问题)此时烧杯中的溶质成分是什么?
(猜想与假设)Ⅰ:Na2SO4;Ⅱ:_____________;Ⅲ:Na2SO4和NaOH。
(实验与探究)
实验步骤 | 实验现象 | 实验结论 |
取少量上述烧杯中的溶液于试管中,滴加_______溶液 | _______________ | 猜想Ⅱ正确 |
取少量上述烧杯中的溶液于试管中,滴加_______溶液 | ______________ | 猜想Ⅲ正确 |