题目内容
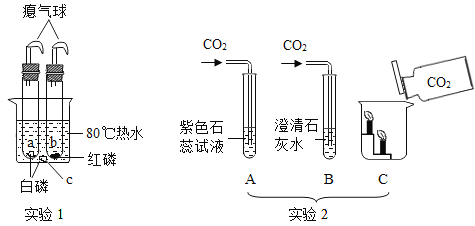
【题目】请结合下图回答问题:
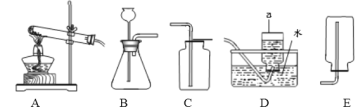
(1)标号a的仪器名称___________。
(2)实验室用氯酸钾和二氧化锰制取氧气的化学方程式为________,选用A、D装置制取O2,A装置中试管口略向下倾斜的原因是__________________,可用D装置收集O2的原因是__________________。
(3)写出实验室用大理石与稀盐酸反应制取二氧化碳的化学方程式________________________,用排空气法收集二氧化碳,可选用的收集装置为___________(填字母)。
(4)工业上可用煅烧石灰石制得二氧化碳,若要制取7.7t二氧化碳,需要含碳酸钙87.5%的石灰石质量是多少?(假设杂质不反应)___________
【答案】集气瓶  防止冷凝水回流到热的试管底部,炸裂试管 不易溶于水且不与水反应 CaCO3+2HCl=CaCl2+H2O+CO2↑ C 20t
防止冷凝水回流到热的试管底部,炸裂试管 不易溶于水且不与水反应 CaCO3+2HCl=CaCl2+H2O+CO2↑ C 20t
【解析】
(1)集气瓶是常用的反应容器,标号a的仪器名称集气瓶;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,化学方程式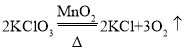 ;选用A、D装置制取O2,A装置中试管口略向下倾斜的原因是:防止水倒流而炸裂试管;氧气不易溶于水且不与水反应,因此能用排水法收集;
;选用A、D装置制取O2,A装置中试管口略向下倾斜的原因是:防止水倒流而炸裂试管;氧气不易溶于水且不与水反应,因此能用排水法收集;
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑。二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;
(3)解:需要碳酸钙的质量为x,

![]()
解得 x=17.5t
需要含碳酸钙87.5%的石灰石质量是17.5t÷87.5%=20t
答:需要含碳酸钙87.5%的石灰石质量为20t。

 名校课堂系列答案
名校课堂系列答案【题目】在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表。下列关于此反应的认识,正确的是
物 质 | X | Y | Z | W |
反应前的质量(g) | 20 | m | 16 | 14 |
反应后的质量(g) | 4 | 6 | 60 | 50 |
A.m的数值为64
B.若W为水,则X或Y必定为酸或碱
C.参加反应的X与Y的质量比为1︰4
D.若X为化合物,Y为单质,则该反应一定为置换反应