题目内容
【题目】化学实验是学习化学的基础,请分别回答下列问题.
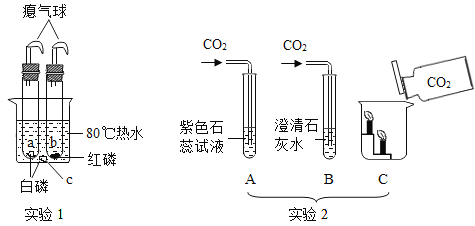
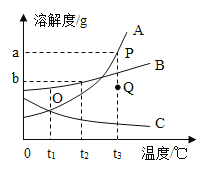
(1)通过实验1可以探究燃烧的条件.烧杯中有热水,a、b、c三个位置分别放有药品,可以观察到a处的现象是:白磷燃烧,产生大量__,放出热量.实验1中气球的作用是__.__与__(填编号)对比,说明燃烧需要的条件是可燃物需要与氧气接触;__与__(填编号)对比,说明燃烧的条件是温度要达到可燃物的着火点.
(2)实验2包括A、B、C三个小实验.
A:往紫色石蕊试液中通入干燥的CO2,可以观察到的现象是__.
B:往澄清石灰水中通入干燥的CO2,可以观察到的现象是__,该反应的化学方程式为__.
C:把二氧化碳气体慢慢倒入放着燃着的蜡烛的烧杯中,低的蜡烛先熄灭,高的蜡烛后熄灭,说明二氧化碳具有__、不能燃烧和不支持燃烧的性质.
【答案】白烟 防止生成的P2O5颗粒污染空气 a c a b 紫色石蕊试液变红 石灰水变浑浊 CO2+Ca(OH)2=CaCO3↓+H2O 密度比空气大
【解析】
(1)白磷燃烧,冒出大量的白烟;实验1中气球的作用是防止生成的P2O5颗粒污染空气;a中的白磷与氧气接触,且温度达到了着火点,所以燃烧;b中的红磷虽然与氧气接触,但是温度没有达到其着火点,所以没有燃烧;c处的白磷温度虽然达到了其着火点,但是没有与氧气接触,所以没有燃烧;由上述分析可知,a与c对比,说明燃烧需要的条件是可燃物需要与氧气接触,a与b对比,说明燃烧的条件是温度要达到可燃物的着火点;
(2)A:向紫色石蕊溶液中通入二氧化碳生成了碳酸,碳酸能使石蕊溶液变为红色;
B:向足量的澄清石灰水中通入二氧化碳,会观察到石灰水变浑浊,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,其化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
C:把二氧化碳气体慢慢倒入放有燃着的蜡烛的烧杯中,下层蜡烛先灭,说明二氧化碳具有密度比空气大、不燃烧和不支持燃烧的性质。

 名校课堂系列答案
名校课堂系列答案【题目】下列图像不能正确反映对应变化关系的是
|
|
|
|
A.将水通电电解一 段时间 | B.加热一定量的高 锰酸钾固体 | C.向两份相等质量的块状大理石和粉末状大理石中分别加入过量的等浓度的稀盐酸 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D
【题目】学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:Fe2O3能否起到类似MnO2的催化剂作用呢?于是进行了以下探究.
(猜想)I.Fe2O3是反应的催化剂,反应前后__;
II.Fe2O3参与反应产生O2,反应前后质量和化学性质发生了改变;
III.Fe2O3不是催化剂、也不参与反应,反应前后质量和化学性质不变.
(查阅资料)Fe2O3属于碱性氧化物,能够与稀盐酸反应生成氯化铁;氯化铁溶液显棕黄色.
(实验)用天平称量 0.3gFe2O3,取5mL5%的过氧化氢溶液于试管中,进行如下实验:
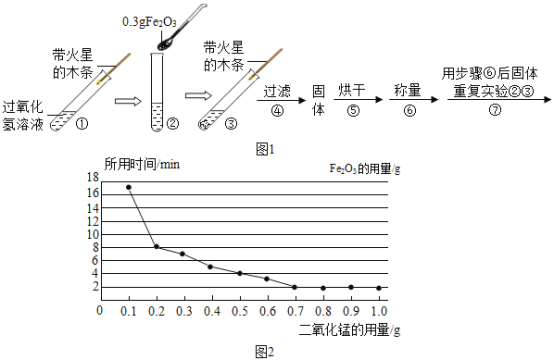
(1)填写下表:
步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
__,带火星的木条复燃. | __ | 溶液中有气泡放出, __ | 猜想I成立; 猜想II、III不成立. |
(2)步骤①的目的是__.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、__.
(4)过氧化氢能被Fe2O3催化分解放出O2的化学方程式为__.
(拓展)
(1)要探究步骤⑤做过催化剂的Fe2O3其它化学性质,还应补做的实验是__(写一种).
(2)该同学为了探究Fe2O3的用量对H2O2分解速率的影响.每次均用30mL 10%的H2O2溶液,使用不同质量的Fe2O3作催化剂,测定每次收集到500mL O2所用的时间.结果如图(其他实验条件相同),由图可知,Fe2O3的用量对H2O2分解速率影响的规律是:
①__;
②Fe2O3的用量超出一定范围后,其用量再增大,反应速率不再继续加快.
【题目】在探究铝化学性质时发现铝与稀盐酸反应比与稀硫酸反应剧烈,化学兴趣小组进行了如下探究:
(1)铝与稀盐酸反应的化学方程式为_____。
(2)铝片使用前需要打磨的原因是_____,铝能被用来制作导线是因为其具有_____性。
(3)实验过程中,可以通过观察_____来比较铝与稀盐酸和稀硫酸反应的剧烈程度。
(4)(作出猜想)猜想一:Cl-对反应起了促进作用;
猜想二:SO![]() 对反应起了阻碍作用;
对反应起了阻碍作用;
猜想三:以上两种猜想同时成立。
(进行实验)
实验 | 实验操作 |
实验1 | 将铝片加入到10mLpH=1的稀盐酸中,然后向其中滴加CuSO4溶液 |
实验2 | 将铝片加入到10mLpH=1的稀硫酸中,然后向其中滴加浓盐酸 |
实验3 | 将铝片加入到10mLpH=1的稀盐酸中,然后向其中滴加Na2SO4溶液 |
(分析并得出结论)
①同学们认为实验1不可行,理由是_____。
②同学们认为实验2思路不正确,改进的方法是_____。
③实验3没有明显现象,证明猜想_____不成立。