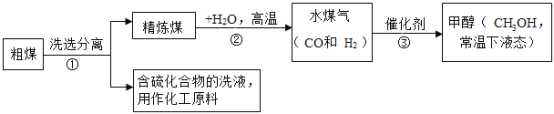
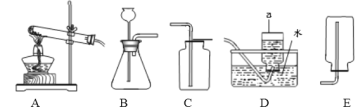
题目内容
【题目】水是生命之源,人类的生产、生活离不开水.
(1)在利用太阳能使水分解的过程中,太阳能转化为_____能.
(2)用洗洁精洗去餐具上的油污,洗洁精起_____作用.
(3)我国规定生活饮用水的水质必须达到下述4项指标,通过过滤可达到_____(填标号)指标.
A无异色 B无异味 C澄清透明 D无细菌和病毒
(4)甲、乙两种物质的溶解度曲线图如图所示.
①在10℃时,两种物质的溶解度比较:甲_____乙(填“>”“<”或“=”).
②t1℃时,将80g甲物质放入100g 水中,充分搅拌,形成的是_____(填“饱和溶液”或“不饱和溶液”),该溶液的溶质质量分数为_____.

【答案】化学 乳化 C < 饱和溶液 37.5%
【解析】
(1)太阳能使水分解,故太阳能转化为了化学能,故填:化学;
(2)洗洁精中含有乳化剂,乳化剂具有乳化作用,能将油污乳化为细小油滴随水冲走,故填:乳化;
(3)通过过滤能除去水中的不溶性固体杂质,可以使水变得澄清透明,故填:C;
(4)①根据图象可以看出,在10℃时,甲的溶解度小于乙,故填:<;
②t1℃时,甲的溶解度是60g,将80g甲物质放入100g 水中,充分搅拌,只能溶解60g,故形成的是饱和溶液;
该溶液的溶质质量分数为![]() ;故填:饱和溶液; 37.5%。
;故填:饱和溶液; 37.5%。

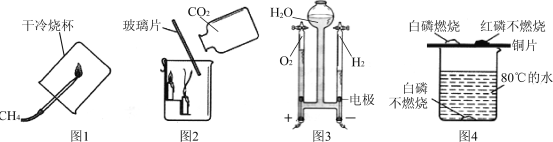
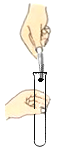
【题目】有如下图所示的两个实验:
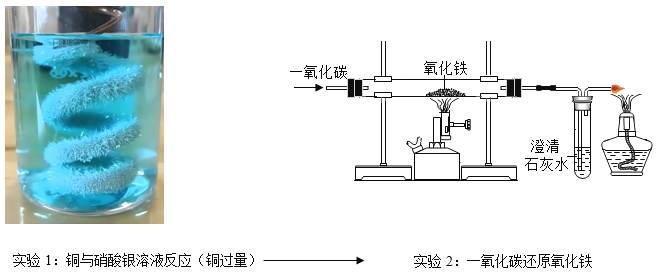
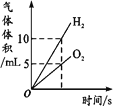
(1)在实验 2 中,加热硬质玻璃管时,管中发生反应的化学方程式为_____。
某同学取一些实验 1 反应后的溶液和一些实验 2 反应后硬质玻璃管中的固体,将它们一同倒入容器M 中,发现有明显变化现象产生,且最终还有固体存在。他对 M 中反应后的物质成分进行如下探究。
(查阅资料)Fe2O3 + 6HCl = 2FeCl3 + 3H2O(FeCl3 溶液呈黄色);Fe2O3 与 Cu(NO3)2 不反应。
(实验分析)M 中一定发生了的反应的化学方程式是_____。
(提出猜想)反应后,M 中剩余的固体是什么?
猜想Ⅰ:Cu 和 Fe 猜想Ⅱ:Cu 和 Fe2O3 猜想Ⅲ:______。
(进行实验)进行如下实验,请完成填空。
实验步骤 | 实验现象 | 实验结论 |
一、把 M 中反应后的混合物过滤, 得到固体和溶液,将固体烘干, 用磁铁吸引固体。 | ______ | 固体中不含铁。 |
二、再取少量步骤一的固体,加 入过量的稀盐酸。 | 固体减少,溶液变成黄色 | 固体中一定含有_____。 |
(问题探讨)
(2)从 M 中滤出的固体不含单质铁的原因是_________。
(3)如果要进一步确定容器 M 滤出的溶液中是否含有硝酸铜,可用 __________(填试剂名称) 进行检验,通过 __________的现象来进行判断。
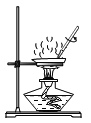
【题目】下列图像不能正确反映对应变化关系的是
|
|
|
|
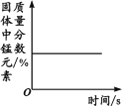
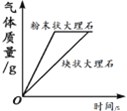
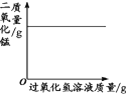
A.将水通电电解一 段时间 | B.加热一定量的高 锰酸钾固体 | C.向两份相等质量的块状大理石和粉末状大理石中分别加入过量的等浓度的稀盐酸 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D
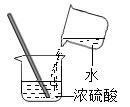
【题目】(7分)某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题。
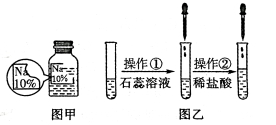
【猜想与假设】其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种。
【资料查阅】上述四种物质的相关信息如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下某稀溶液的pH | 7 | 13 | 11 | 9 |
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是 ;
在进行操作②时有无色无味得到气体产生,由此又可排除假设物质中的 。
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的 ,你的判断依据是 。
【探究反思】
(1)若上述探究结论是正确的,操作②产生的气体应是 (写化学式),实验室检验该气体的实验操作及现象是 。
(2)另有同学猜想其中的溶质还可能是Na2SO4,但又没有Na2SO4的上述表列信息。
请你根据以上实验操作的相关现象,判断该溶液中的溶质是否是Na2SO4,并叙述理由: 。