题目内容
【题目】请沿用科学家认识事物的方式认识“空气”。
(1)从分类角度:空气属于_____(填“混合物”或“纯净物”)。
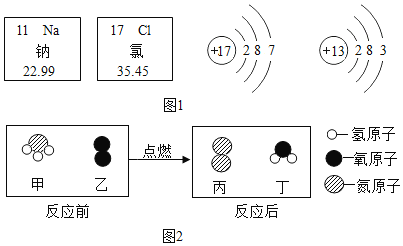
(2)从微观角度:用“![]() ”表示氮原子,“
”表示氮原子,“![]() ”表示氧原子。
”表示氧原子。
①用“![]() ”可表示的微粒是_____(填“名称”)。
”可表示的微粒是_____(填“名称”)。
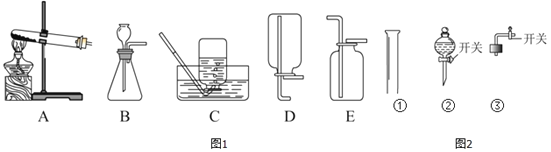
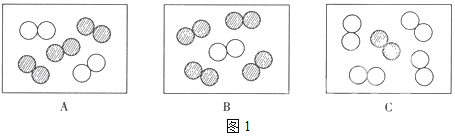
②同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,图1可表示空气微观模型的是_____(填“选项字母”)。
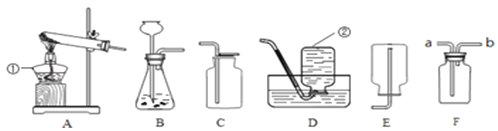
(3)从变化角度:利用空气制取氮肥的流程如图2所示。
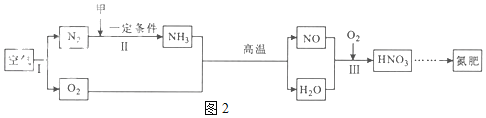
①变化Ⅰ属于_____(填“物理”或“化学”)变化。
②变化Ⅱ中参加反应的甲一定含有的原子是_____。
③变化Ⅲ所属的基本反应类型为_____(填“化合”或“分解”)。
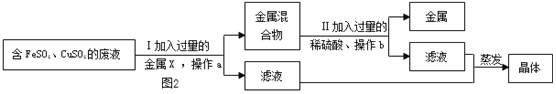
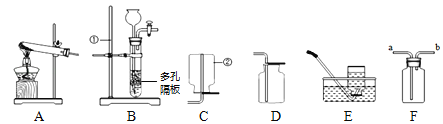
(4)从定量的角度:测定氧气的含量如图3所示。
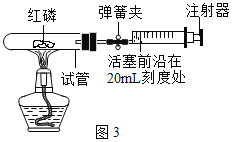
①实验前,打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明_____。
②写出红磷燃烧的符号表达式:_____。
③根据下表提供的实验数据(反应后,打开弹簧夹),完成下表。
反应前试管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 20mL | 13mL | _____ |
【答案】混合物 氮分子 C 物理 氢原子 化合 整个装置都不漏气 P+O2![]() P2O5 15.6%。
P2O5 15.6%。
【解析】
(1)空气是由氮气、氧气、稀有气体、二氧化碳等多种物质组成的,属于混合物,故填混合物。
(2)①分子是由原子构成的,用“![]() ”可表示的微粒是由两个氮原子构成的氮分子,故填氮分子;
”可表示的微粒是由两个氮原子构成的氮分子,故填氮分子;
②氧气约占空气体积的![]() ,氮气约占空气体积的
,氮气约占空气体积的![]() ,则空气中氮气与氧气的体积比为4:1,所以氮分子与氧分子的个数比也为4:1,所以图中可表示空气微观模型的是C,故填C。
,则空气中氮气与氧气的体积比为4:1,所以氮分子与氧分子的个数比也为4:1,所以图中可表示空气微观模型的是C,故填C。
(3)①变化Ⅰ只是将空气中的氮气与氧气进行了分离,没有生成新物质,属于物理变化,故填物理;
②由质量守恒定律可知,化学反应前后,原子的种类与数目保持不变,反应Ⅱ生成物氨气分子中含有氮原子和氢原子,反应物氮气分子中含有氮原子,所以一定还有氢原子参与反应,故填氢原子;
③变化Ⅲ是一氧化氮、水和氧气反应生成硝酸,是由多种物质反应生成另一种新物质的反应,属于化合反应,故填化合。
(4)①打开弹簧夹,将注射器活塞前沿从20mL刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明整个装置都不漏气,故填整个装置都不漏气;
②磷与氧气在点燃的条件下反应生成五氧化二磷,故反应的符号表达式写为:P+O2![]() P2O5;
P2O5;
③注射器内气体减少的体积为消耗的氧气的体积,即20mL﹣13mL=7mL,空气的总体积为25mL+20mL=45mL,所以实验测得空气中氧气的体积分数为:![]() ,故填15.6%。
,故填15.6%。

【题目】泡腾片配料表如下:
成分 | 柠檬酸 | 碳酸氢钠 | 维生素C | 乳糖 | 色素香精 |
每片含量(4 g/片) | 未知 | 未知 | 0.2 g | 未知 | 极少量 |
泡腾片放入温开水中,浮于水面上,产生大量气泡,所得溶液喝起来酸甜可口。已知:柠檬酸的化学式为C6H8O7,相对分子质量为192;泡腾片溶于水时,碳酸氢钠刚好与柠檬酸完全反应,生成Na3C6H5O7。
(1)泡腾片在水中产生气体的化学式为_____。泡腾片中柠檬酸与碳酸氢钠的质量比为_____。
(2)称取5.00 g泡腾片放入200.00 g温开水中,待泡腾片完全溶解,不再产生气体后,测得溶液质量为203.68 g.通过计算确定泡腾片中柠檬酸的质量分数_____。
【题目】某实验小组利用废硫酸液制备K2SO4

(1)将CaCO3研成粉末的目的是 .
(2)上述流程中可循环使用的物质有CO2和 (填写化学式).
(3)反应Ⅲ中相关物质的溶解度如下表.你认为反应Ⅲ在常温下能实现的原因是
物质 | KCl | K2SO4 | NH4Cl | M |
溶解度/g(25℃) | 34.0 | 11.1 | 37.2 | 19.5 |
(4)不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是 ;为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入 (选填序号,下同),振荡、静置,再向上层清液中滴加 ,观察现象即可判断.
a.AgNO3溶液 b.过量的BaCl2溶液 c.过量的Ba(NO3)2溶液