题目内容
【题目】请你仔细分析如图所示的实验过程和所提供的数据,并进行计算。(写出具体计算过程)
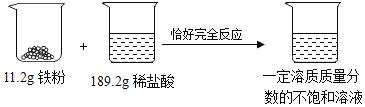
(1)生成氢气的质量__________g?
(2)反应后所得溶液中溶质的质量分数是__________?
【答案】由题意,11.2g铁粉与189.2g稀盐酸恰好完全反应,设生成的氢气的质量为x,则有:
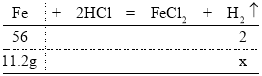
由![]() 解得x=0.4g;
解得x=0.4g;
答:生成氢气的质量为0.4g; 由题意,11.2g铁粉与189.2g稀盐酸恰好完全反应,设生成的绿化亚铁的质量为y,则有:

由![]() 解得y=25.4g;
解得y=25.4g;
结合生成氢气的质量为0.4g,反应后所得溶液中溶质的质量分数是![]()
答:反应后所得溶液中溶质的质量分数是12.7%。
【解析】
由题意,11.2g铁粉与189.2g稀盐酸恰好完全反应,设生成的氢气的质量为x,生成的绿化亚铁的质量为y,则有:

由![]() 解得x=0.4g;
解得x=0.4g;
由![]() 解得y=25.4g;
解得y=25.4g;
(1)生成氢气的质量为0.4g;
(2)反应后所得溶液中溶质的质量分数是![]() 。
。
答:(1)生成氢气的质量为0.4g;
(2)反应后所得溶液中溶质的质量分数是12.7%。

练习册系列答案
相关题目