题目内容
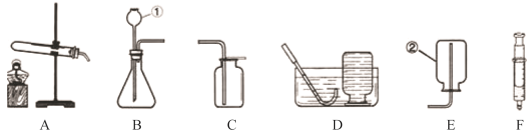
【题目】在实验室,利用下列装置可以制取某些气体,请回答下列问题:
(1)写出编号的仪器名称:①_____________________;②______________________。
(2)利用B装置可制取多种气体。装入药品前,可用注射器F检查装置B的气密性,步骤如下:
①向锥形瓶中加水至_____________________以形成液封;
②将注射器F连接到装置B的出气导管口处;
③缓慢拉动注射器F的活塞,观察到_________________,表示装置B的气密性良好。
(3)若实验室用B装置制取氧气,则反应的化学方程式是__________________,可选用D装置收集氧气,其原因是____________________。
(4)实验室用加热氯酸钾和二氧化锰来制取氧气,发生装置应选择______(填编号)。反应的化学方程式是________________。
(5)实验室常用稀盐酸和石灰石反应制CO2,该反应的化学方程式________________;收集装置为_________。检验CO2的化学方程式为________________;
【答案】长颈漏斗 集气瓶 浸没长颈漏斗下端管口 长颈漏斗下端管口有气泡冒出 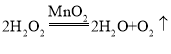 氧气不易溶于水 A
氧气不易溶于水 A 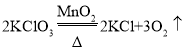 CaCO3+2HCl=CaCl2+H2O+CO2↑ C Ca(OH)2+CO2=CaCO3↓+H2O
CaCO3+2HCl=CaCl2+H2O+CO2↑ C Ca(OH)2+CO2=CaCO3↓+H2O
【解析】
(1)标号①的装置是长颈漏斗,标号②的装置是集气瓶。故答案为:长颈漏斗、集气瓶;
(2)①使用长颈漏斗时,应该将液体药品浸没长颈漏斗下端,以形成液封,避免生成的气体逸出。故答案为:浸没长颈漏斗下端管口;
③用注射器检查装置的气密性时,向锥形瓶中加入少量的水至浸没长颈漏斗下端管口,将注射器F连接到装置B的右侧导管处,缓慢拉都注射器F的活塞,则锥形瓶中的气体被抽出。若装置气密性良好,则外界大气压将会压着空气沿着长颈漏斗进入锥形瓶中,从而观察到长颈漏斗末端有气泡逸出。故答案为:长颈漏斗下端管口有气泡冒出;
(3)实验室使用B装置制取氧气,B装置是固液混合不加热法,实验室利用固液混合不加热法制取氧气的过氧化氢在二氧化锰的催化作用下分解产生水和氧气。收集氧气时可以使用排水法收集,是因为氧气不易溶于水。故答案为: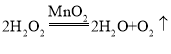 、氧气不易溶于水;
、氧气不易溶于水;
(4)实验室使用氯酸钾制取氧气,氯酸钾在二氧化锰的催化作用下,在加热的条件下分解,分解出氯化钾和氧气。氯酸钾和二氧化锰都是固体,所以实验室制取的发生装置应该选择固固混合加热法。故答案为:A、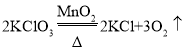 ;
;
(5)实验室使用固体药品石灰石和液体药品稀盐酸在常温下接触,即可反应生成二氧化碳。石灰石中的碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳。因为二氧化碳的密度比空气大且二氧化碳能溶于水,所以二氧化碳只能用向上排空气法来收集。检验二氧化碳用的是澄清的石灰水。澄清的石灰水的主要成分是氢氧化钙,氢氧化钙和二氧化碳反应生成难溶于水的碳酸钙沉淀和水。故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑、C、Ca(OH)2+CO2=CaCO3↓+H2O。

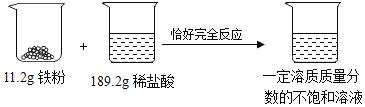
【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是______。
(2)试计算这种石灰石中碳酸钙的质量分数_______。
【题目】在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如表所示。已知X的相对分子质量为n,Q的相对分子质量为2n,则下列推断正确是( )
物质 | X | Y | Z | Q |
反应前质量 | 4g | 10g | 1g | 21g |
反应后质量 | 0g | 12g | 15g | 待测 |
A.Q是生成物
B.反应后Q的质量为12g
C.该反应化学方程式中X与Q的化学计量数之比为2:3
D.反应后生成15gZ