题目内容
【题目】某兴趣小组对一氧化碳还原氧化铁的相关知识进行了深入研究。
(知识回顾)写出一氧化碳还原氧化铁的化学方程式______________________。
(提出问题)该小组同学发现甲烷的性质与氢气、一氧化碳有很多相似之处。氢气、一氧化碳具有还原性,那么甲烷有没有还原性呢?
(查阅资料)1无水硫酸铜是白色固体,吸收水分后变为蓝色。
2铁与稀硫酸反应生成硫酸亚铁和氢气,铁的氧化物与稀硫酸反应时无气体生成
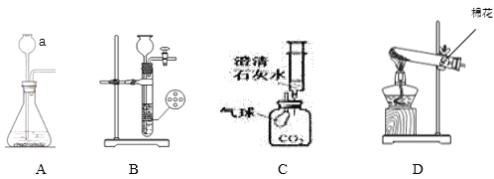
(实验探究)为探究上述问题,设计如下装置并进行实验。
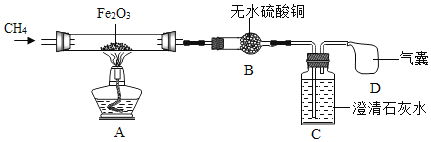
(1)实验开始时先通一段时间甲烷的目的是_________________。
(2)加热一段时间后,观察到A中硬质玻璃管中的固体粉末由红色全部变成黑色,取少量黑色粉末于试管中,加入适量稀硫酸,观察到_____(填实验现象),说明有铁生成;B中白色固体变蓝,说明有_____生成;C中澄清石灰水变浑浊,说明有二氧化碳生成。
(结论)甲烷有还原性,若生成的黑色粉末全部是铁,甲烷还原氧化铁的化学方程式为_____________。
(反思质疑)查阅资料得知:酒精灯加热时达不到高温,生成物中可能混有铁的其他氧化物FexOy.为探究甲烷与氧化铁反应后所得黑色粉末的成分,继续进行如下实验:
(1)探究黑色粉末中单质铁的质量分数:
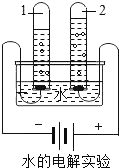
①将图1各装置按照一定顺序连接,接口顺序是a→_____→_____→d(填序号)。
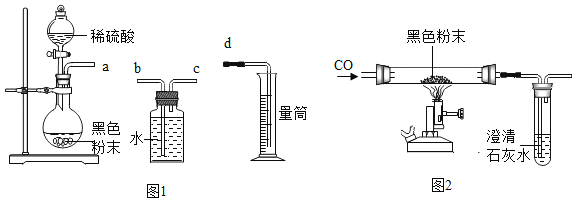
②检查装置气密性,称取7.2g黑色粉末 放入烧瓶中,向分液漏斗中加入稀硫酸。打开分液漏斗活塞,逐滴加入稀硫酸至无气泡产生,通过测量量筒内水的体积得出氢气质量为0.05g。计算黑色粉末中单质铁的质量分数_________。(写出计算过程,结果保留到0.1%)(Fe + H2SO4=FeSO4 + H2↑)
(2)确定黑色粉末中FexOy的化学式:检查图2装置的气密性,另称取上述黑色粉末7.2g放入硬质玻璃管中,加热至完全反应,称得硬质玻璃管内剩余固体为5.6g,经检验全都是铁。若原黑色粉末中铁的氧化物只有一种,则FexOy的化学式为________。从环保角度分析,图2装置存在的明显缺陷是__________。
【答案】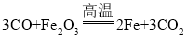 排尽装置内的空气,防止加热时发生爆炸 有气泡产生 水
排尽装置内的空气,防止加热时发生爆炸 有气泡产生 水 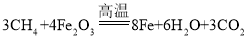 c b 19.4% FeO 没有进行尾气的处理
c b 19.4% FeO 没有进行尾气的处理
【解析】
[知识回顾]
一氧化碳与氧化铁在高温条件下反应生成铁和二氧化碳,故化学方程式为: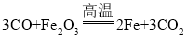 ;
;
[实验探究]
(1)通入的甲烷具有可燃性,甲烷与空气的混合气体加热可能发生爆炸,故实验开始时先通一段时间甲烷的目的是排尽装置内的空气,防止加热时发生爆炸,故填:排尽装置内的空气,防止加热时发生爆炸;
(2)取少量黑色粉末于试管中,加入适量稀硫酸,反应后生成的黑色粉末中,若有铁,加入稀硫酸,铁与稀硫酸反应生成氢气,故观察到有气泡产生,说明有铁生成;B中装有白色的无水硫酸铜固体,资料中提供:无水硫酸铜是白色固体,吸收水分后变为蓝色;B中白色固体变蓝,说明有水生成,故填:有气泡产生;水;
[结论]
根据上述实验,甲烷与氧化铁反应生成铁、水和二氧化碳,故甲烷还原氧化铁的化学方程式为: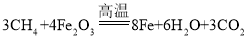 ;
;
[反思质疑]
(1)①铁和稀硫酸反应生成的硫酸亚铁和氢气,使用排水法收集,则气体从短管进入,故接口顺序是a→c→b→d,故填:c;b;
②检查装置气密性,称取7.2g黑色粉末 放入烧瓶中,向分液漏斗中加入稀硫酸。打开分液漏斗活塞,逐滴加入稀硫酸至无气泡产生,通过测量量筒内水的体积得出氢气质量为0.05g。
设生成0.05g氢气,需铁的质量为X
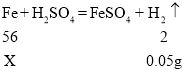
![]()
X=1.4g
故黑色粉末中单质铁的质量分数=![]() ;
;
(2)取上述黑色粉末7.2g放入硬质玻璃管中,加热至完全反应,称得硬质玻璃管内剩余固体为5.6g,故氧元素的质量=7.2g-5.6g=1.6g,则铁元素和氧元素的原子个数比为:![]() :
:![]() =1:1,故FexOy的化学式为FeO;从环保角度分析,图2装置是用一氧化碳还原黑色粉末,一氧化碳能与血液中的血红蛋白结合,造成人体缺氧(有毒),一氧化碳不能与澄清的石灰水反应,在装置中的尾气没有处理。
=1:1,故FexOy的化学式为FeO;从环保角度分析,图2装置是用一氧化碳还原黑色粉末,一氧化碳能与血液中的血红蛋白结合,造成人体缺氧(有毒),一氧化碳不能与澄清的石灰水反应,在装置中的尾气没有处理。
故填:FeO;没有进行尾气的处理。

 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案【题目】为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学分别用质量分数相同的盐酸与样品充分反应进行实验测定。已知,样品中的杂质不溶于水,且不与盐酸反应。测得数据如下表:
甲 | 乙 | 丙 | 丁 | |
所取石灰石样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
加入盐酸的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
剩余固体的质量/g | 6.0 | m | 2.0 | n |
请回答:
(1)甲同学实验中碳酸钙_____剩余(有,或者没有)。
(2)石灰石样品中碳酸钙的质量分数是_____;(精确到0.1%)
(3)10.0 g样品与足量稀盐酸反应后可产生二氧化碳多少克? _____(写出计算过程,计算结果精确到0.1 g)(可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40)
【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是______。
(2)试计算这种石灰石中碳酸钙的质量分数_______。