题目内容
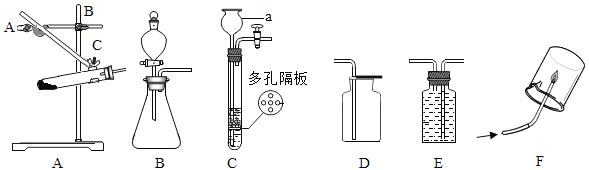
【题目】已知铁有三种氧化物,如FeO、Fe2O3、Fe3O4,在一定条件下,均能失去其中的氧,被还原为铁。现有仅含Fe、O两种元素的固体14.4g,为了探究其成分进行如图所示的实验。充分反应后,称得装置C在反应前后质量增加了8.8g.下列说法正确的个数有( )个
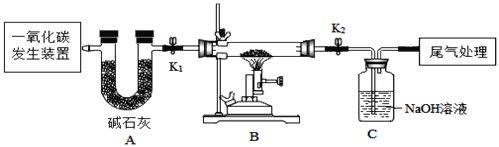
(通入A装置中的CO气体混有CO2和H2O,碱石灰能完全吸收CO2和H2O,NaOH溶液能完全吸收CO2)
①实验开始前应先点燃酒精喷灯,再通入一氧化碳气体。
②若无A装置,测定的原固体中铁元素质量分数将偏大
③根据实验数据进行计算,可确定原固体中铁和氧的原子的个数比为1:1
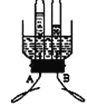
④B中反应停止时为防止B中固体被氧化,应关闭K1、K2
⑤原14.4克固体的组成可能有7种情况。
A.1B.2C.3D.4
【答案】B
【解析】
装置C在反应前后质量增加了8.8g,即生成的二氧化碳质量为8.8g。
设样品中氧元素的质量为x,则

![]() ,则铁元素质量为14.4g-3.2g=11.2g;
,则铁元素质量为14.4g-3.2g=11.2g;
①实验开始前应先通入一氧化碳气体,再点燃酒精喷灯,防止发生爆炸,错误。
②若无A装置,测得生成二氧化碳的质量偏大,测定的原固体中氧元素的质量分数偏大,则铁元素质量分数将偏小,错误。
③原固体中铁和氧的原子的个数比为![]() ,正确;
,正确;
④B中反应停止时为防止B中固体被氧化,应关闭K1、K2,并防止氢氧化钠溶液倒流,正确;
⑤原固体中铁和氧的原子的个数比为1:1,符合条件只有氧化亚铁,错误。
故正确的有③④;故选:B。

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案【题目】为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学分别用质量分数相同的盐酸与样品充分反应进行实验测定。已知,样品中的杂质不溶于水,且不与盐酸反应。测得数据如下表:
甲 | 乙 | 丙 | 丁 | |
所取石灰石样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
加入盐酸的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
剩余固体的质量/g | 6.0 | m | 2.0 | n |
请回答:
(1)甲同学实验中碳酸钙_____剩余(有,或者没有)。
(2)石灰石样品中碳酸钙的质量分数是_____;(精确到0.1%)
(3)10.0 g样品与足量稀盐酸反应后可产生二氧化碳多少克? _____(写出计算过程,计算结果精确到0.1 g)(可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40)