题目内容
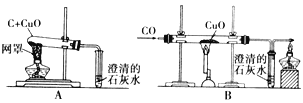
【题目】物质的性质决定着物质在生产和生活中的用途。木炭和一氧化碳都具有还原性,可用于冶炼金属。请根据下图回答:
(1)请写出下列反应的化学方程式:
①木炭还原氧化铜:_____。②二氧化碳与澄清石灰水的反应:_____。
(2)A装置中网罩的作用是_____;B装置最右端酒精灯的作用是_____。
(3)A、B装置中均能观察到的现象是①_____;②_____。
(4)A装置试管口略向下倾斜,其目的是_____;实验结束后,应先将导管撤去,后熄灭酒精灯,其目的是_____;一氧化碳有可燃性,点燃前要_____。因此,在实验开始时,要先通_____,目的是_____。
【答案】C+ 2CuO![]() 2Cu + CO2↑ CO2 +Ca(OH)2 =CaCO3↓+ H2O 使酒精灯火焰集中,提高温度 尾气点燃,防止其污染空气 黑色粉末变成红色 澄清石灰水变浑浊 防止冷凝水倒流,引起试管的炸裂 防止石灰水倒流,引起试管的炸裂 检验纯度 一氧化碳 排尽空气,防止爆炸
2Cu + CO2↑ CO2 +Ca(OH)2 =CaCO3↓+ H2O 使酒精灯火焰集中,提高温度 尾气点燃,防止其污染空气 黑色粉末变成红色 澄清石灰水变浑浊 防止冷凝水倒流,引起试管的炸裂 防止石灰水倒流,引起试管的炸裂 检验纯度 一氧化碳 排尽空气,防止爆炸
【解析】
(1)①木炭与氧化铜在高温条件下反应生成二氧化碳和铜,反应的化学方程式为:木炭还原氧化铜:C+ 2CuO![]() 2Cu + CO2↑;
2Cu + CO2↑;
②二氧化碳与澄清石灰水的反应生成碳酸钙和水,反应的化学方程式为:CO2 +Ca(OH)2 =CaCO3↓+ H2O;
(2)A装置中网罩的作用是使酒精灯火焰集中,提高温度;一氧化碳有毒,不能直接排放空气中,一氧化碳在空气中燃烧生成二氧化碳,B装置最右端酒精灯的作用是将尾气点燃,防止其污染空气;
(3)A、B装置中均能观察到的现象是①黑色粉末变成红色;②澄清石灰水变浑浊;
(4)A装置试管口略向下倾斜,其目的是防止冷凝水倒流,引起试管的炸裂;实验结束后,应先将导管撤去,后熄灭酒精灯,其目的是防止石灰水倒流,引起试管的炸裂;一氧化碳有可燃性,为防止爆炸,点燃前要检验纯度。因此,在实验开始时,要先通一氧化碳,目的是排尽空气,防止爆炸。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】为了检测石灰石样品中碳酸钙的含量,甲、乙、丙、丁四位同学分别用质量分数相同的盐酸与样品充分反应进行实验测定。已知,样品中的杂质不溶于水,且不与盐酸反应。测得数据如下表:
甲 | 乙 | 丙 | 丁 | |
所取石灰石样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
加入盐酸的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
剩余固体的质量/g | 6.0 | m | 2.0 | n |
请回答:
(1)甲同学实验中碳酸钙_____剩余(有,或者没有)。
(2)石灰石样品中碳酸钙的质量分数是_____;(精确到0.1%)
(3)10.0 g样品与足量稀盐酸反应后可产生二氧化碳多少克? _____(写出计算过程,计算结果精确到0.1 g)(可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40)
【题目】石灰石是常见的主要矿石之一,学校研究性学习小组为了测定某矿山石灰石中碳酸钙的质量分数,取来一些矿石样品,并取来稀盐酸200g,平均分成4份,进行实验,结果如下:
实验 | 1 | 2 | 3 | 4 |
加入样品的质量(g) | 5 | 10 | 15 | 20 |
生成CO2的质量(g) | 1.76 | 3.52 | 4.4 | m |
(1)表中m的数值是______。
(2)试计算这种石灰石中碳酸钙的质量分数_______。
【题目】如图是关于碳元素的相关信息

(1)金刚石和石墨都是由碳元素组成,但物理性质却有很大差异,因为_____。图中 a、b 物质含有共同的离子,离子符号为_____
(2)下图为某科学小组进行木炭还原氧化铜的部分实验装置,数据如表。
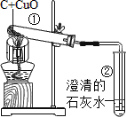
反应前的质量 | 反应后的质量 | |
试管①和药品总质量 | 56.0g | 53.8g |
a.过关开始预热,试管②中立即产生气泡,但石灰水不变浑浊,一段时间后,石灰石变浑浊。预热时,石灰石不变浑浊的原因是_____。
b.请根据化学式计算,参加反应的氧化铜的质量是多少克_____?