题目内容
【题目】如图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
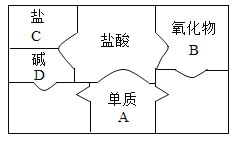
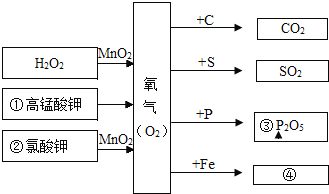
(1)下列物质中[a.Mg b.Fe c.Ag d.Zn]A不可能是______(填标号)
(2)若C为碳酸钠
①C与D的反应属于______(填基本反应类型)
②D与盐酸反应的化学方程式为______(写一个)
【答案】c 复分解反应 2HCl+Ca(OH)2=CaCl2+2H2O
【解析】
(1)A为金属单质,金属活动顺序表中氢前面的金属和盐酸反应,氢后面的金属和稀盐酸不反应,a、b、c、d中的金属Mg、Fe、Zn和盐酸反应,银和盐酸不反应;
故答案为:c;
(2)①C是碳酸钠,能与碱反应生成新的盐和新的碱,属于复分解反应,故填:复分解反应;
②D是能与碳酸钠反应的碱,可以是碱氢氧化钙,能与盐酸反应生成氯化钙和水,故填:2HCl+Ca(OH)2═CaCl2+2H2O。

【题目】将宏观、微观及化学符号相联系是化学学习的特点。下图中表格是元素周期表的部分信息,A、B、C、D是四种粒子的结构示意图,请回答下列问题。
11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.07 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
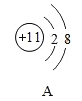
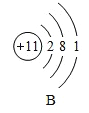
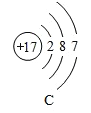
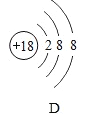
(1)硫原子的核外电子数为______;
(2)在四种粒子中,易得到电子,成相对稳定结构的是______,它们所对应的元素种类有______种;
(3)图A所示的粒子可用化学符号表示为______。
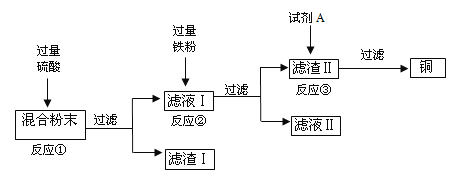
【题目】现有H2SO4和CuSO4的混合溶液,为了测定CuSO4的质量分数,小明同学进行如下实验:
取混合溶液于烧杯中,向其中加入铁片至完全反应。反应前后,有关数据如表。
烧杯 | 原混合溶液 | 加入的铁片 | 反应后烧和烧杯内物质的总质量(克) | 剩余铁片 | 析出铜 | |
质量(克) | 80 | 100 | 20 | 199.8 | 3.2 | 12.8 |
(1)实验中产生氢气的质量为______克。
(2)请根据实验数据计算原混合溶液中CuSO4的质量分数______。
(3)小红同学用加入足量BaCl2溶液,通过生成BaSO4沉淀的质量来计算原混合溶液中CuSO4的质量分数,请分析是否合理并说明原因______。
【题目】某兴趣小组对食用纯碱和食用小苏打两种粉末进行以下探究.
[查阅资料]
名称 | 食用纯碱 | 食用小苏打 |
主要成分 | Na2CO3 | NaHCO3 |
酸碱性 | 水溶液显碱性 | 水溶液显碱性 |
热稳定性 | 受热不分解 | 270℃时完全分解为碳酸钠、二氧化碳、水 |
[实验探究]
(1)探究两者水溶液酸碱性的差异
小明分别向等浓度的两种溶液中滴入酚酞试液,发现两者都变_____色,但食用纯碱溶液中颜色更深,由此推测可能_____溶液碱性更强.小欢认为要比较两种溶液的碱性强弱,可直接用_____进行测定.
(2)验证两种粉末的稳定性
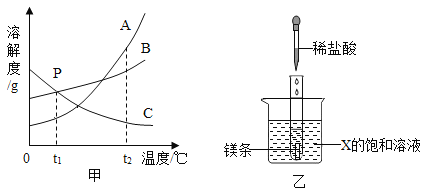
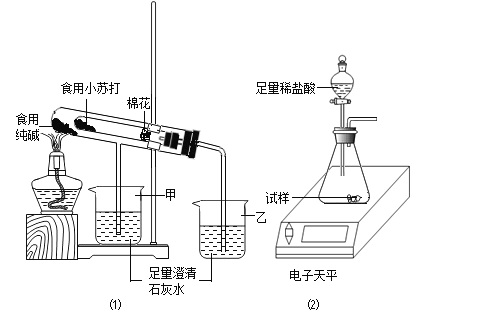
在老师的指导下,该小组按如图1装置进行实验操作,观察到_____(填“甲”或“乙”)烧杯中澄清石灰水变浑浊,试管中发生反应的化学方程式为_____,装置中棉花的作用是_____.
(3)测定食用纯碱粉末的纯度
取食用纯碱粉末试样,利用如图2装置进行实验测定.
数据记录如下:
称量项目 | 称量时间 | 质量/g |
试样 | 11.0 | |
装置+稀盐酸 | 160.0 | |
装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
①反应生成CO2的质量为_____g.
②通过计算确定食用纯碱粉末中Na2CO3的质量分数____.(写出计算过程,结果保留一位小数.)
③如果测得的结果比实际纯度高,可能的原因是_____.(答一种即可)