题目内容
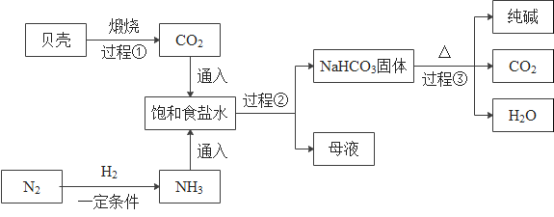
【题目】我国制碱工业先驱侯德榜发明了“侯氏制碱法”其模拟流程如下:
[小资料]
I .贝壳的主要成分是CaCO3;
II.通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳;
Ⅲ.饱和食盐水中发生的主要反应为![]() ,
,![]() (NaHCO3由于饱和后析出,变成沉淀)。
(NaHCO3由于饱和后析出,变成沉淀)。
(1)过程②中主要操作的名称是__________________。
(2)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入NH3后通入CO2,你的理由是__________________。
(3)上述流程中可以循环利用的物质是_________________(填化学式)。
【答案】过滤 氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有利于生成较多的碳酸氢钠 CO2
【解析】
碳酸钙煅烧生成氧化钙和二氧化碳,碳酸氢钠加热生成碳酸钠、水和二氧化碳,氮气和氢气在一定条件下生成氨气。
(1)过程②是将碳酸氢钠固体与氯化铵溶液分离,故主要操作的名称是过滤。
(2)氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有利于生成较多的碳酸氢钠,故为了提高产率,往饱和食盐水中通入气体时,应该先通入NH3后通入CO2,理由是氨气在水中的溶解度大,先通氨气会吸收更多的二氧化碳,有利于生成较多的碳酸氢钠。
(3)从反应过程看出将二氧化碳通过氨盐水制取碳酸氢钠和氯化铵,碳酸氢钠分解生成二氧化碳,二氧化碳可循环利用,故流程中可以循环利用的物质是二氧化碳,化学式为CO2。

【题目】超市出现了一种名为“污渍爆炸盐”的新产品,能在瞬间去除洗衣粉难以除去的多种顽固污渍。某校化学兴趣小组的同学们在老师的指导下对该产品开展了以下探究活动。

(阅读标签)本产品不含_____,环保。
(查阅资料)①“污渍爆炸盐”的主要成分是过碳酸钠(Na2CO4),它是一种白色结晶颗粒,易溶于水。且能与水反应,生成碳酸盐和其他化合物。
②氢氧化镁是不溶于水的白色固体。
(提出问题)“污渍爆炸盐”溶于水形成的溶液溶质是什么?
(作出猜想)猜想一:Na2CO3和H2O2
猜想二:Na2CO3和NaOH
猜想三:Na2CO3、H2O2和NaOH
(实验探究)
序号 | 实验步骤 | 实验现象 | 实验结论 |
① | 取少量“污渍爆炸盐”于烧杯中,加入足量蒸馏水充分搅拌 | 固体完全溶解形成无色溶液 | |
② | 取适量①的溶液于试管中,先向其中加入少量二氧化锰粉末,再将带火星的木条置于试管口 | 有大量气泡产生,木条复燃 | 含有_____ |
③ | 取_____振荡,静置 | 有白色淀产生 | 含有碳酸钠 |
④ | 取适量③的上层清液于试中,向其中滴加少量氯化镁溶液,振荡 | 清液中_____ | 不含氢氧化钠 |
(得出结论)猜想_____正确。
请写出过碳酸钠与水反应的化学方程式:_____。
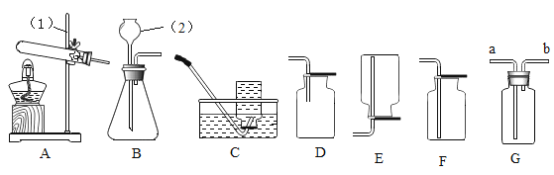
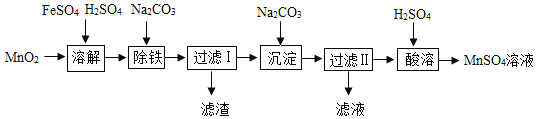
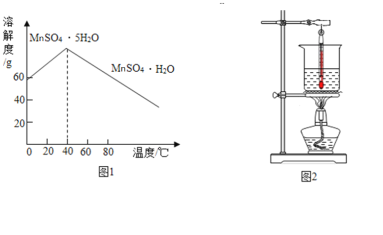
(延伸拓展)同学们进一步对“污渍爆炸盐”中过碳酸钠的含量进行测定,经讨论设计了如下图所示的实验装置。图中装置B盛装氢氧化钠溶液,C盛装澄清石灰水,D盛装浓硫酸,E、F均装入干燥的碱石灰(主要成分:氧化钙和氢氧化钠的固体混合物;可吸收二氧化碳和水蒸气)。
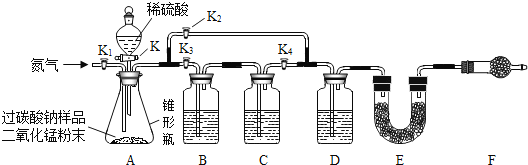
①称量装置E的质量;②组装好装置,检查气密性,装入药品;③关闭活塞K,打开活塞K1,通入氮气;④关闭活塞K、K2,打开活塞K1、K3、K4,通入一段时间的氮气;⑤依次关闭活塞K1、K3、K4,打开活塞K、K2,直到反应不再进行;⑥再次称量装置E的质量。以上实验步骤的正确顺序是_____。
A ①②③④⑤⑥
B ②①④⑤③⑥
C ①②④⑤③⑥
D ②④①⑤③⑥
【题目】下列图象与所述实验相符的是( )
A | B | C | D |
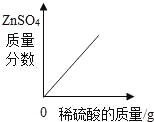
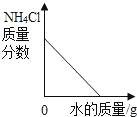
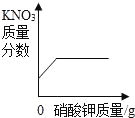
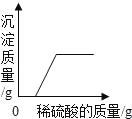
向一定量锌粒中加入过量稀硫酸 | 向一定量氯化铵饱和溶液中不断加入水 | t℃时,向一定量不饱和的硝酸钾溶液中不断加入硝酸钾晶体 | 向一定量氢氧化钠和氢氧化钡的混合溶液中加入稀硫酸 |
|
|
|
|
A. AB. BC. CD. D