题目内容
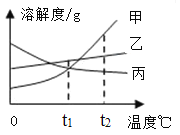
【题目】下列图象与所述实验相符的是( )
A | B | C | D |
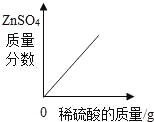
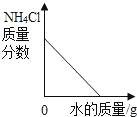
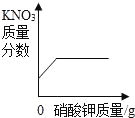
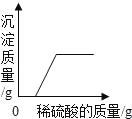
向一定量锌粒中加入过量稀硫酸 | 向一定量氯化铵饱和溶液中不断加入水 | t℃时,向一定量不饱和的硝酸钾溶液中不断加入硝酸钾晶体 | 向一定量氢氧化钠和氢氧化钡的混合溶液中加入稀硫酸 |
|
|
|
|
A. AB. BC. CD. D
【答案】C
【解析】
A、因为锌的质量一定,所以随着硫酸的加入,锌反应完全,当锌反应完全后,硫酸锌溶液的质量分数将慢慢减小,因为溶液的质量随着稀硫酸的不断加入而不断增加,而硫酸锌的质量不再增加,所以硫酸锌溶液的质量分数应该会慢慢减小(但不会到零),所以A错误;
B、向饱和氯化铵溶液不断加水,氯化铵溶液的质量分数将不断减小,但不会降为0,所以B错误。
C、温度一定,溶解度一定,溶液的溶质质量分数一定。t℃时,硝酸钾变为饱和溶液时,硝酸钾就不能再溶解了,所以硝酸钾的质量分数增大到一定程度就不再增大了,所以C正确。
D、钡离子一旦遇到硫酸就应该产生沉淀的,所以不能为一段时间无沉淀,所以D很明显错误。
故选:C。

【题目】液化石油气是家庭常用燃料,主要成分是丙烷和丁烷.
性质 物质 | 熔点/℃ | 沸点/℃ | 燃烧反应 |
丙烷 | ﹣189.7 | ﹣42.1 | C3H8+5O2 |
丁烷 | ﹣138.4 | ﹣0.5 | 2C4H10+13O2 |
(1)由上表资料分析,丙烷和丁烷的物理性质是:常温常压下呈_____态(填“气”、“液”或“固”);化学性质是:具有_____ 性.
(2)液化石油气燃烧需要大量的氧气,根据化学方程式计算:59g丁烷充分燃烧所需要的氧气的质量_____.
(3)已知含碳气体的含氢量越高,相同条件下充分燃烧时产生CO2就越少. 比较甲烷、丙烷和丁烷分子中氢的质量分数,看出最洁净的燃料是_____(填化学式).
(4)气体燃料具有价廉、使用方便等优点,但使用时应特别注意安全问题.
①若灶具上的风板调节不好,空气供应不足,燃烧不充分,其后果是_____、_____.
②烧水或做饭时,人不要远离灶具.如果火焰熄灭而又没有及时关闭燃气灶,可燃性气体会在厨房里扩散,遇明火会发生_____的危险.
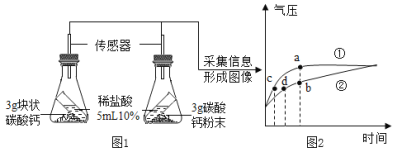
【题目】化学小组同学在查阅“氢氧化钠使酚酞变红的原因”时,看到了以下资料。
①实验室所用酚酞溶液pH<8.酚酞的分子结构受pH影响,酚酞溶液的颜色受其分子结构影响,具体情况如下表所示。
溶液的pH | 1≤pH<8 | 8≤pH≤13 | pH>13 |
酚酞的分子结构 | 内酯式 | 醌式 | 羧酸式 |
酚酞溶液的颜色 | 无色 | 红色 | 无色 |
②醌式结构的酚酞能与H2O2溶液发生反应,生成无色物质,且该物质在溶液中的颜色不受pH影响。
③NaOH溶液浓度越大,溶液pH越高。
该小组同学对上述资料产生了兴趣,决定对酚酞溶液颜色的变化开展探究。
(进行实验)
组别 | 实验操作 | 实验现象及数据 |
1 | 1﹣1:配制pH=13的NaOH溶液,取5 mL于试管中,向其中滴加2滴酚酞溶液后,分成两等份 | |
1﹣2:向一支试管中加入稀盐酸 | 溶液红色褪去 | |
1﹣3:向另一支试管中加入 | 溶液红色褪去 | |
2 | 2﹣1:分别配制pH=8、10、11、13的NaOH溶液,各取5 mL分别加入4支试管中,再分别向4支试管中加入5滴30% H2O2溶 液,最后各滴入2滴酚酞溶液 | 溶液都先变成红色,然后红色逐渐褪去,四支试管变化情况见图:
|
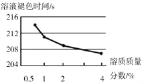
2﹣2:配制pH=9的NaOH溶液,分别取5 mL加入4 支试管中,再向各试管中加入5滴质量分数分别为0.5%、1%、2%、4%的H2O2溶液,最后各滴入2滴酚酞溶液 | 溶液都先变成红色,然后红色逐渐褪去,四支试管变化情况见图:
|
(解释与结论)
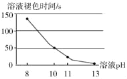
(1)实验1﹣1中,可以观察到的实验现象是_____。
(2)实验1﹣2中,溶液红色褪去的原因是_____(用化学方程式表示)。
(3)实验1﹣3的目的是验证pH>13时,红色酚酞溶液会变成无色,则“向另一支试管中加入______。”
(4)由实验2﹣1可以得到结论:H2O2能使变红的酚酞褪色,_____。
(5)实验2﹣2的目的是_____。