题目内容
【题目】用化学符号或化学符号中数字表示的意义填空。
(1)氨气__________。
(2)3个氮分子_________。
(3)2个硫酸根离子___________。
(4)氯酸钾中氯元素的化合价_________。
(5)3SO3中“3”的意义分别是:前“3”表示____。后“3”表示_____。
【答案】NH3 3N2 2SO42- ![]() 3个三氧化硫分子 1个三氧化硫分子中含有3个氧原子
3个三氧化硫分子 1个三氧化硫分子中含有3个氧原子
【解析】
(1)氨气的化学式为:NH3;
(2)分子用化学式表示,多个分子就是在化学式前面加上相应的数字,故3个氮分子为:3N2;
(3)离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;故2个硫酸根离子为:2SO42-;
(4)氯酸钾中钾元素的化合价为+1价,氧元素的化合价为-2价,设氯元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:(+1)+x+(-2)×3=0,x=+5,元素化合价的表示方法是在化学式该元素的上方用正负号和数字表示,正负号标在数字前面,故氯酸钾中氯元素的化合价表示为:![]() ;
;
(5)位于化学式前面的数字:表示几个分子,故前“3”表示3个三氧化硫分子;
位于化学式中元素符号(或原子团)右下角的数字,表示一个分子中所含的原子或原子团的个数,故后“3”表示,1个三氧化硫分子中含有3个氧原子。

 阅读快车系列答案
阅读快车系列答案【题目】为探究盐酸的化学性质,某化学小组做了如下实验:
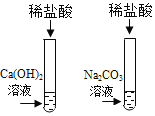
将反应后两只试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行探究。
[提出问题]滤液中溶质的成分是什么?
[假设与猜想]猜想一: NaCl
猜想二: NaCl 和CaCl2
猜想三: NaCl、Ca(OH)2 和HCl
猜想四:___________。
[讨论与交流]经讨论同学们一致认为猜想_________是错误的。原因是____________(用化学方程式解释)
[实验与结论]
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量碳酸钠溶液 | 无现象 | 猜想四成立 |
取少量滤液于试管中,滴加适量_______________ | ______________________ |
[拓展与迁移]稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在_______________。