题目内容
【题目】(8分)已知碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,而碳酸钠受热不分解.现有某工厂生产出的一批碳酸氢钠中混有少量的碳酸钠,为了测定产品中碳酸氢钠的质量分数,具体的检验步骤如下:
①取一只洁净的坩埚,称其质量为a g;再向其中加入样品。称得总质量为m1 g;
②加热该盛有样品的坩埚;
③将坩埚充分冷却,称量坩埚和剩余固体的质量;
④多次重复步骤②和③至恒重,称得坩埚和剩余固体的总质量为m2 g。
(1)写出碳酸氢钠受热分解的化学方程式 ▲ 。
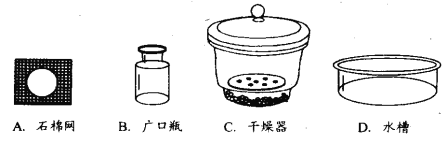
(2)用 ▲ (填仪器名称)将加热后的坩埚放到 ▲ 中(填序号)冷却。
(3)根据题意,用a、m1、m2的代数式表示样品中碳酸氢钠的质量分数为 ▲ 。
(4)步骤①、③和④都需要用到精度为0.1g的托盘天平称量,若本题中(m1-m2)的值超过0.6g,假设样品中碳酸氢钠的质量分数为90%,则至少需称样品多少克?▲
【答案】(1)2NaHCO3====Na2CO3+H2O+CO2↑
(2)坩埚钳 C
(3)![]() 或
或![]()
(4)取样量为1.8g
【解析】(1)根据信息:碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,写出碳酸氢钠受热分解的化学方程式;
(2)为防止加热后物质在冷却过程中吸收空气中水而影响测定结果,应放在干燥器中进行冷却;
(3)根据质量守恒定律,由加热前后剩余物质的质量差可求得分解反应出二氧化碳与水的质量即固体减少的质量,由固体减少的质量根据化学方程式计算出样品中碳酸氢钠质量,并进一步计算样品中碳酸氢钠的质量分数;
(4)根据假设样品中碳酸氢钠的质量分数为90%及固体减少的质量0.6g,由样品中碳酸氢钠的质量分数的代数式,计算出至少需称样品的质量.
解答:解:(1)碳酸氢钠在270℃左右就能分解为碳酸钠、水和二氧化碳,反应的化学方程式为2NaHCO3![]() Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
(2)使用坩埚钳把加热后的坩埚移入干燥器C中进行冷却,防止冷却过程中吸收空气中的水分,而影响后面的称量的结果;
(3)设样品中碳酸氢钠的质量为x
2NaHCO3![]() Na2CO3+H2O+CO2↑ 固体质量减少
Na2CO3+H2O+CO2↑ 固体质量减少
168106 168-106=62
x m1-m2![]() =
=![]()
x=![]()
样品中碳酸氢钠的质量分数=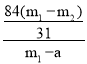 ×100%=
×100%=![]()
故答案为:
(1)2NaHCO3![]() Na2CO3+H2O↑+CO2↑;
Na2CO3+H2O↑+CO2↑;
(2)坩埚钳;C;
(3)![]() ;
;
(4)![]() ×100%=90%
×100%=90%
(m1-a)=![]() ≈1.8g
≈1.8g

 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案【题目】武汉将成为我国首个新型氢能城市。某化学兴趣小组在老师的帮助下围绕氢气的燃烧实验开展如下探究:
(1)点燃氢气前,一定先要________。点燃纯净的氢气可以看到淡蓝色火焰现象,该反应的化学方程式为________,该反应的基本类型为______反应。
(2)研究氢气燃烧实验,需要用试管收集不同体积比的氢气与空气的混合物,若用试管(假设试管容积为10mL)收集氢气与空气体积比为4:1的混合气体,其操作方法为________。
(3)用不同体积比的混合气体做氢气的燃烧实验,结果如表:
序号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
氢气与空气体积比 | 9:1 | 8:2 | 7:3 | 5:5 | 3:7 | 1:9 | 0.5:9.5 |
点燃现象 | 安静 燃烧 | 安静 燃烧 | 弱的 爆鸣声 | 强的 爆鸣声 | 强的 爆鸣声 | 弱的 爆鸣声 | 不燃烧 不爆鸣 |
请分析上表信息,你对燃烧或燃烧条件的新认识是可燃物能否燃烧除具备燃烧条件,还要考虑到________。