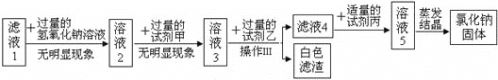
��Ŀ����
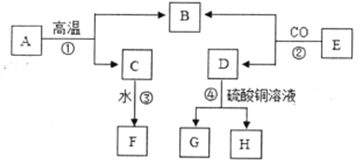
����Ŀ���������������������������й㷺��Ӧ����
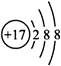
(1)���Ƹ�����÷��ͷ��к���̼�����ƣ�������Ϊ__________( ����ĸ����)��
a������ b���ռ� c���մ� d��С�մ�
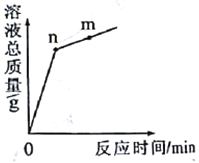
(2)��ͼ������������Һ�����ᷴӦʱ��ҺpH�仯��ʾ��ͼ��

�ٸ���ͼʾ�жϣ���ʵ���ǽ�______ ( ��������������Һ������������)�μӵ���һ����Һ����
�ڵ�����Һ���ΪV2mLʱ,��Һ�е�����Ϊ__________��
(3)Ϊ��ȥ����ˮ�еĿ���������MgSO4��CaCl2��ij��ѧС����������·�����
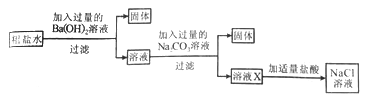
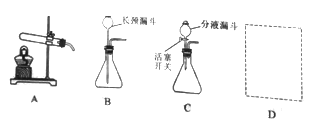
�ٹ����õ��IJ����������ձ�����������__________��
��д������Ba(OH)2��Һʱ��Ӧ�Ļ�ѧ����ʽ___________ ( ��ʾ�����ﲻ�γɳ���)
����ҺX�к�����Щ����? __________�����ʵ�����֤����(��Ҫд��ʵ�鲽�������) ___________
(4)Ϊ�ⶨijʯ��ʯ��Ʒ��̼��Ƶ�������������ȡ10gʯ��ʯ(���ʲ��μӷ�Ӧ)�����ձ��У�����100gϡ���ᣬ����ǡ����ȫ��Ӧ����Ӧ���ձ����������ʵ�������Ϊ106.7 g(������ܽ���Բ���)����������Ʒ��̼��Ƶ���������Ϊ___________��
���𰸡� d ���� Na2SO4��H2SO4 ©�� MgSO4+Ba(OH)2=Mg(OH)2��+BaSO4�� NaOH ��Na2CO3 ȡ������ҺX���Թ��У��������CaCl2����BaCl2����Һ�����ְ�ɫ����������(�����)�����ϲ���Һ������Һ���еμӷ�̪��Һ������Һ��졣 75%
��������(1)����̼�������׳�С�մ���(2) �ٸ�����Һ��pH�ɴ���7��С��С��7������𣻢ڸ�����Һ��pH��7�������Խ��(3) �ٸ��ݹ��˲�����Ҫ�IJ����������ձ�����������©����𣻢ڸ�������þ������������Һ��Ӧ���������ᱵ��������þ��𣻢۸���ԭ���κ����Ȼ��ƺ�����þ�������������������Һ���ȥ����þ���ټ��������̼������Һ����ȥ�Ȼ��ƺ��������������������������Ʒ������(4)���ݷ�Ӧ�Ļ�ѧ����ʽ��������(1)̼�������׳�С�մ�����ѡd��(2) ������Һ��pH�ɴ���7��С��С��7��֪����ʵ���ǽ�����μӵ���һ����Һ��������Һ��pH��7�������ԣ�����Һ�е�����ΪNa2SO4��H2SO4��(3) �ٹ����õ��IJ����������ձ�����������©����������þ������������Һ��Ӧ���������ᱵ��������þ����Ӧ�Ļ�ѧ����ʽΪMgSO4+Ba(OH)2=Mg(OH)2��+BaSO4������ԭ���κ����Ȼ��ƺ�����þ�������������������Һ���ȥ����þ���ټ��������̼������Һ����ȥ�Ȼ��ƺ��������������������������ơ�����ҺX�е�������NaOH ��Na2CO3��������ȡ������ҺX���Թ��У��������CaCl2��Һ�����ְ�ɫ����������Na2CO3�����ã�ȡ�ϲ���Һ������μӷ�̪��Һ������Һ��죬��˵������NaOH��(4)���ɶ�����̼������=10g+100g-106.7g=3.3g������Ʒ��̼��Ƶ�����Ϊx��
CaCO3+2HCl=CaCl2+H2O+CO2��
100 44
x 3.3g
![]()
x=7.5g
����Ʒ��̼��Ƶ���������Ϊ![]() ��100��=75��
��100��=75��
�𣺸���Ʒ��̼��Ƶ���������Ϊ75����

 ��У����ϵ�д�
��У����ϵ�д�