题目内容
【题目】某兴趣小组同学在实验室用自来水配制氢氧化钠溶液时,发现溶液中有白色浑浊物.对此现象小组同学都感到疑惑,于是进行了如下探究.
(提出问题)白色浑浊物是什么物质?
(查阅资料)①自来水是硬水,常常含有Ca(HCO3)2 和Mg(HCO3)2.
②Ca(HCO3)2 能与氢氧化钠反应:Ca(HCO3)2+2NaOH=CaCO3↓+2H2O+Na2CO3
Mg(HCO3)2能与氢氧化钠反应:Mg(HCO3)2+2NaOH=Mg(OH)2↓+2H2O+Na2CO3
③Mg(OH)2在热水中溶解度增大,可形成稀溶液.
(作出猜想)猜想一:白色浑浊物是CaCO3猜想二:白色浑浊物是Mg(OH)2
猜想三:白色浑浊物是___.
(实验探究)
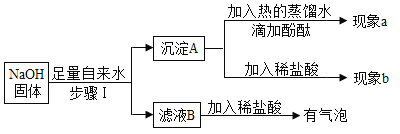
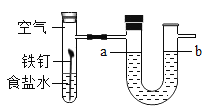
(1)步骤Ⅰ中,发现杯壁发烫,原因是 ___.
(2)若现象a酚酞溶液不变色,现象b有气泡冒出,则猜想___正确,有关反应的化学方程式是___.
(3)若___、___,则猜想三正确.
(拓展延伸)(1)小红同学认为滤液B中只含有Na2CO3,但小霞同学认为滤液B中还可能存在NaOH.于是,小霞取少量滤液B于试管中,滴加无色酚酞溶液,发现酚酞溶液变红,证明滤液B中确实有NaOH.
小薇认为由小霞的实验得出的结论不正确,理由是___.
为了证明NaOH确实存在,请你写出对小霞实验方案的改进措施___.
(2)写出从该滤液B中得到纯NaOH溶液的化学方程式___.
(实验反思)
(1)实验室在配制溶液时,应该使用___水.
(2)判断自来水是硬水的方法是___.
【答案】CaCO3和Mg(OH)2 氢氧化钠溶解放出热量 一 CaCO3+2HCl═CaCl2+H2O+CO2↑ 现象a液体变红 现象b有气泡冒出 碳酸钠溶液显碱性,也能使无色酚酞溶液变红 在加入无色酚酞溶液之前,先加入足量的氯化钙溶液或氯化钡溶液以除去碳酸钠的干扰 Na2CO3+Ca(OH)2═CaCO3↓+2NaOH 蒸馏(或纯) 加肥皂水振荡,产生泡沫较少(或较多浮渣)
【解析】
根据查阅资料:自来水是硬水,常含有Ca(HCO3)2 和Mg(HCO3)2;Ca(HCO3)2+2NaOH=CaCO3↓+2H2O+Na2CO3,
Mg (HCO3)2+2NaOH=Mg(OH)2↓+2H2O+Na2CO3,及氢氧化钠溶解放出热量,而Mg(OH)2在热水中溶解度增大,可推测猜想三:白色浑浊物是白色浑浊物是CaCO3和Mg(OH)2;
[实验探究](1)取氢氧化钠于烧杯中,加自来水水搅拌,杯壁发烫,原因是:氢氧化钠溶解放出热量;
(2)Mg(OH)2在热水中溶解度增大,可形成稀溶液,显碱性,若现象a酚酞溶液不变色,说明不含氢氧化镁;现象b有气泡冒出,说明含有碳酸钙,猜想一正确;碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;
③若猜想三是正确的,既有碳酸钙,又有氢氧化镁,需要现象a液体变红;现象b有气泡冒出;
[拓展延伸](1)碳酸钠溶液显碱性,也能使无色酚酞溶液变红,不能证明有氢氧化钠;改进方法:在加入无色酚酞溶液之前,先加入足量的氯化钙溶液或氯化钡溶液以除去碳酸钠的干扰;
(2)要得到纯NaOH溶液就需要将碳酸钠除去,可加入适量的氢氧化钙溶液;化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
[实验反思](1)通过上述实验可知实验室在配制溶液时应该使用蒸馏水(或纯水);
(2)鉴别自来水是硬水的方法是在自来水中加肥皂水,振荡,产生泡沫较少。