题目内容
【题目】结合下列实验装置,回答问题。
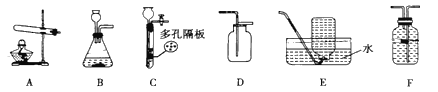
(1)写出选用装置A制取氧气的化学方程式_______。
(2)制取CO2时,只能选用装置D收集CO2的理由是什么_______?
(3)若用装置B和装置F来制取H2,请将图补充完整。_______
【答案】2KMnO4![]() K2MnO4+MnO2+O2↑ CO2密度比空气大,且易溶于水
K2MnO4+MnO2+O2↑ CO2密度比空气大,且易溶于水 
【解析】
(1)实验室用高锰酸钾法制氧气通常选用装置A,高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,化学方程式2KMnO4![]() K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑;
(2)制取CO2时,只能选用装置D收集CO2的理由是CO2密度比空气大,且能溶于水,不能用向下排空气法或排水法收集;
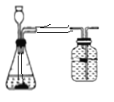
(3)若用装置B和装置F来制取H2,应将长颈漏斗末端伸入液面以下,氢气的密度比水的小,氢气从短管进入F瓶,装置如图:

练习册系列答案
相关题目
【题目】为了测定混有少量杂质的高锰酸钾固体样品中高锰酸钾的质量分数,取20g样品加热(杂质不反应),剩余固体的质量与加热时间的关系如表所示:
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
剩余固体质量/g | 20 | 20 | 19.6 | 18.8 | 18.6 | 18.4 | 18.4 |
(1)t0至t1时间段,固体质量不变的原因是____________________________。
(2)反应中产生氧气的质量是_________。
(3)求样品中高锰酸钾的质量分数_________。
(4)该反应中转化为氧气的氧元素质量占高锰酸钾中氧元素质量的________%。