题目内容
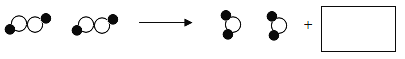
【题目】将37.2g 某种天然气水合物(CH4-xH2O)与一定量氧气在密闭容器中用电火花引燃,反应后得到二氧化碳、一氧化碳和水蒸气的混合气体的总质量为53.2g ,冷却至室温剩余气体的质量为10.0g ,下列说法中正确的是( )
A.x=8
B.上述反应消耗氧气的质量为26.0g
C.该天然气水合物中碳、氢元素的原子个数比为1:18
D.若要使上述37.2g 天然气水合物充分燃烧至少需要19.2g氧气
【答案】D
【解析】
A.由题意可知,反应生成水的质量为:53.2g-10g=43.2g,根据化学反应前后元素种类和质量均不变,生成水中的氢元素质量等于反应物天然气水合物中的氢元素质量,则:![]() ,解得:x=6,说法错误;
,解得:x=6,说法错误;
B.由质量守恒定律可知,参加反应的氧气质量为:52.3g-37.2g=16g,说法错误;
C.由上述A计算可知,该天然气水合物的化学式为,由该化学式可知,该天然气水合物中碳、氢元素的原子个数比为:1:16,说法错误;
D.使上述天然气水合物充分燃烧生成物是二氧化碳和水,设充分燃烧需要氧气质量为y,则
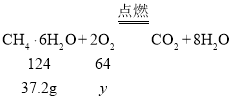
![]()
y=19.2g;
若要使上述37.2g 天然气水合物充分燃烧至少需要19.2g氧气,说法正确。
故选:D。

 名校课堂系列答案
名校课堂系列答案【题目】如图是某品牌化肥标签,为了验证该化肥的含氮量,分析和实验如下:
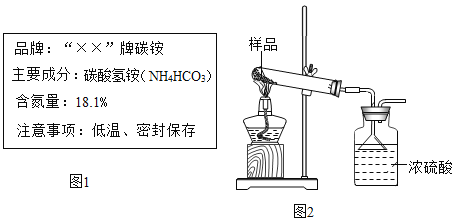
(1)通过列式计算判断此标签是否有错误。计算结果保留至0.1%
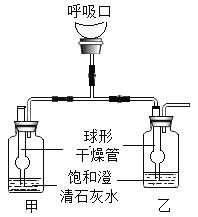
(2)根据国家标准碳铵化肥中碳酸氢铵含量不得低于95%某实验小组为了验证该化肥是否合格,利用图装置进行了三次试验![]() 假设杂质不发生反应
假设杂质不发生反应![]() ,实验结果如下:
,实验结果如下:
实验次数 | 1 | 2 | 3 | 平均值 |
样品的质量 | 16.0 | 16.0 | 16.0 | 16.0 |
浓硫酸增加的质量 | 3.41 | 3.39 | 3.40 | 3.40 |
①小华同学认为反应后浓硫酸增加的质量是氨气的质量,反应为![]()
根据小华的分析,该化肥中碳酸氢铵的质量分数为______计算结果保留至0.1%。
②小青同学认为小华的计算结果不能说明该化肥是否合格,理由是______。根播小青的分析,列式计算该化肥中碳酸氢铵的质量分数,并判断该化肥是否合格。计算结果保留至0.1%
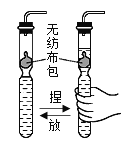
【题目】从Ⅰ~Ⅲ中任选二个作答,若均作答,按前两个计分。用如图装置进行实验(夹持仪器略去,)。
实验 | 按要求回答问题 | ||
用手挤压使固液接触。 | 编号 | 药品 | |
Ⅰ | 大理石 稀盐酸 | 其反应的化学方程式为___ | |
Ⅱ | 铁片 稀硫酸 | 观察到的现象是 _______ | |
Ⅲ | 二氧化锰(颗粒状) 过氧化氢 | 检验有氧气生成的操作是______ | |