题目内容
【题目】结合所学化学知识,回答下列问题:
(1)金属生锈是世界面临的难题。铁生锈实际上是铁与_______共同作用的结果,除去铁锈通常使用_______,反应的化学方程式是________.防止金属腐蚀是保护金属资源的有效途径之一。请再写出一条有效途径_______
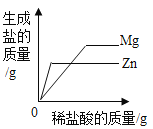
(2)已知M、N、R三种金属存在如下反应:R+NCl2=N+RCl2;M+RCl2=R+MCl2,这两个反应的基本反应类型都是_______,M、N、R三种金属的活动性由强到弱的顺序为_________。
(3)人类的日常生活及工农业生产都与水密切相关,在日常生活中常用________的方法降低水的硬度;自来水厂净化水用到的活性炭其作用是________,在下列净化水的单一操作中,净化程度相对较高的是_______(填选项字母)A静置沉淀 B过滤 C蒸馏;水在通电条件下可以分解,其反应的化学方程式为_________。
(4)在“淀粉、食盐、尿素、熟石灰、羊毛、涤纶、”中选择适当的物质填空:面粉的主要成分是________,用于改良酸性土壤的是________,用作调味品的是_________,用于编织布料的合成有机高分子材料是________。
【答案】氧气和水 稀盐酸 Fe2O3+6HCl=2FeCl3+3H2O 金属的回收和利用、寻找金属的代用品等 置换反应 M>R>N 煮沸 吸附水中的色素和异味 C 2H2O![]() 2H2↑+ O2↑ 淀粉 熟石灰 食盐 涤纶
2H2↑+ O2↑ 淀粉 熟石灰 食盐 涤纶
【解析】
(1)铁生锈实际上是铁与空气中的氧气和水共同作用的结果,铁锈的主要成分是氧化铁,除去铁锈通常使用稀盐酸,稀盐酸和氧化铁反应生成氯化铁和水。反应的化学方程式是Fe2O3+6HCl=2FeCl3+3H2O。防止金属腐蚀是保护金属资源的有效途径之一,保护金属资源的有效途径还有:金属的回收和利用、寻找金属的代用品等。
(2)这两个反应都是由单质与化合物反应生成新的单质与新的化合物,属于置换反应;由金属的活动性可知,排在前面的金属可以将排在后面的金属从其盐溶液中置换出来,R+NCl2=N+RCl2,说明金属活动性R>N ;M+RCl2=R+MCl2,说明金属活动性M>R,故M、N、R三种金属的活动性由强到弱的顺序为M>R>N。
(3)在日常生活中常用煮沸的方法降低水的硬度;自来水厂净化水用到的活性炭其作用是吸附水中的色素和异味,净化程度相对较高的是蒸馏;水在通电条件下可以分解为氢气和氧气,其反应的化学方程式为2H2O![]() 2H2↑+ O2↑。
2H2↑+ O2↑。
(4)在“淀粉、食盐、尿素、熟石灰、羊毛、涤纶、”中选择适当的物质填空:面粉的主要成分是淀粉,熟石灰显碱性常用于改良酸性土壤,食盐常用作调味品,用于编织布料的合成有机高分子材料是涤纶。

 学练快车道口算心算速算天天练系列答案
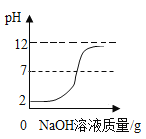
学练快车道口算心算速算天天练系列答案【题目】某石油化工厂化验室的实验员用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,测得实验数据见下表
实验序号 | 消耗NaOH溶液的质量 | 洗涤后溶液的PH值 |
① | 30g | pH>7 |
② | 40g | pH=7 |
③ | 50g | pH<7 |
请回答下列问题:
(1)计算出一定量石油产品中所含H2SO4的质量,你觉得应该选择实验序号______的数据
(2)若该定量石油产品残余硫酸的质量为100g,计算该残余硫酸的溶质质量分数(写出详细的计算过程)
【题目】糕点疏松剂的主要成分有碳酸氢钠(白色固体)。某化学兴趣小组的同学对碳酸氢钠的性质进行了探究。
实验一:探究碳酸氢钠溶液的酸碱性
测量碳酸氢钠溶液的pH,约为10,由此可知碳酸氢钠溶液呈_____性。
实验二:探究碳酸氢钠的热稳定性
(查阅资料)碳酸氢钠受热容易分解,生成水、二氧化碳气体和一种常见的固体物质。
(进行实验)取一定质量的碳酸氢钠放到铜片上加热。如图所示。

(1)加热一段时间后,观察到烧杯内壁有水珠。实验装置中用到了铜片,主要利用了铜的_____性。
(2)在(1)实验的基础上,如何证明烧杯中还有二氧化碳生成_____(请简述实验方案)。
(3)为了确定实验(1)充分加热后的固体产物的成分,该小组同学又进行实验探究。
(提出假设)猜想①可能是Na2CO3;猜想②可能是NaOH
(设计实验)甲同学方案:取少量充分加热后的固体产物于试管中,加适量水配成溶液,滴加几滴酚酞试液,溶液变红,证明猜想②成立。乙同学认为甲方案不合理,他的理由是_____。
乙同学方案:
实验操作 | 实验现象 | 结论 |
取少量充分加热后的固体产物于试管中,_____ | _____ | 假设①成立,假设②不成立 |
(实验结论)NaHCO3受热分解的化学方程式为_____。