题目内容
【题目】如图是某品牌化肥标签,为了验证该化肥的含氮量,分析和实验如下:
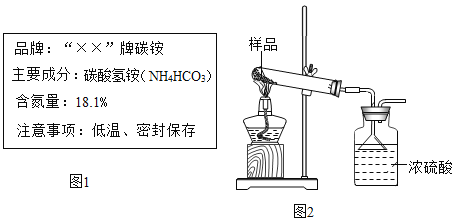
(1)通过列式计算判断此标签是否有错误。计算结果保留至0.1%
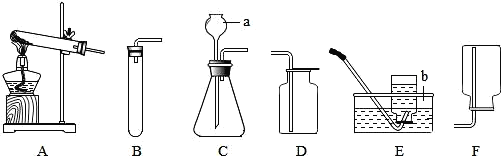
(2)根据国家标准碳铵化肥中碳酸氢铵含量不得低于95%某实验小组为了验证该化肥是否合格,利用图装置进行了三次试验![]() 假设杂质不发生反应
假设杂质不发生反应![]() ,实验结果如下:
,实验结果如下:
实验次数 | 1 | 2 | 3 | 平均值 |
样品的质量 | 16.0 | 16.0 | 16.0 | 16.0 |
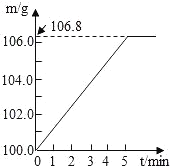
浓硫酸增加的质量 | 3.41 | 3.39 | 3.40 | 3.40 |
①小华同学认为反应后浓硫酸增加的质量是氨气的质量,反应为![]()
根据小华的分析,该化肥中碳酸氢铵的质量分数为______计算结果保留至0.1%。
②小青同学认为小华的计算结果不能说明该化肥是否合格,理由是______。根播小青的分析,列式计算该化肥中碳酸氢铵的质量分数,并判断该化肥是否合格。计算结果保留至0.1%
【答案】(1)17.7%(2)①98.8%②49.0% 该化肥不合格
【解析】
(1)碳酸氢铵中氮元素的质量分数是:![]() ≈17.7%<18.1%,此标签有错误。
≈17.7%<18.1%,此标签有错误。
(2)①小华同学认为反应后浓硫酸增加的质量是氨气的质量,根据图表,氨气的平均质量为:3.40g。
设该化肥中碳酸氢铵的质量为![]() ,
,
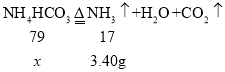
![]()
解得:![]() =15.8g
=15.8g
该化肥中碳酸氢铵的质量分数为:![]() ≈98.8%
≈98.8%
②由题意可知,小青同学认为浓硫酸增加的质量是生成的氨气和水的质量之和为,平均值是3.4g。
设该化肥中碳酸氢铵的质量为![]() ,
,
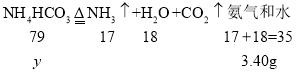
![]()
解得:![]() ≈7.67g
≈7.67g
该化肥中碳酸氢铵的质量分数为:![]() ≈49.0%<95%。
≈49.0%<95%。
所以,该化肥不合格。

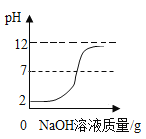
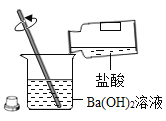
【题目】在实验室,小明将稀盐酸倒入Ba(OH)2溶液中得到溶液甲,相关实验探究如下。
(提出问题)充分反应后所得甲溶液中的溶质是什么?
(合理猜想)(1)氯化钡
(2)氯化钡和盐酸
(3)_____________________。
(实验方案)(4)探究甲溶液中是否含有盐酸?
实验 | 操作 | 现象 | 结论 |
① | 取少量甲溶液于试管中, ______________________。 | 没有气泡产生 | 甲中不含盐酸 |
(5)探究甲溶液中是否含有氢氧化钡?
实验 | 操作 | 现象与化学方程式 | 结论 |
② | 取少量甲溶液于试管中,滴入适量的氯化铁溶液。 | _________ | 甲中含氢氧化钡 |
③用一种试剂一次性确定甲溶液中是否含有氢氧化钡还可用的试剂是___________________。 A纯碱 B盐酸 C氯化铜 D硫酸钠 | |||
(得出结论)(6)通过上面的实验(4)(5)推测,猜想合理的是_______________________。