题目内容
现有氯酸钾和二氧化锰的混合物共26.5g,待反应不再有气体生成后,将试管冷却、称量,得到剩余固体16.9g。求:
⑴制取氧气的质量。
⑵剩余固体中含有哪些物质?各为多少克?
⑴制取氧气的质量。
⑵剩余固体中含有哪些物质?各为多少克?
⑴9.6g;⑵剩余固体为氯化钾和二氧化锰的混合物;MnO2:2g;KCl:14.9g。
分析:根据氯酸钾分解生成氧气的化学方程式可知,只有氧气是气体,则可利用反应前后固体的质量差来计算氧气的质量,然后将氧气的质量代入化学方程式来计算生成的氯化钾的质量来解答.
解答:解:(1)因反应中氧气为气体,则氧气质量为26.5g-16.9g═9.6g,
答:制取氧气的质量为9.6g;
(2)因反应至不再有气体生成,则氯酸钾完全分解,
剩余固体中含氯化钾和二氧化锰,设氯化钾的质量为x,则
2KClO3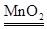 2 KCl+3O2↑
2 KCl+3O2↑
149 96
x 9.6g
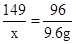 解得x=14.9 g,
解得x=14.9 g,
即氯化钾的质量为14.9g,
则二氧化锰质量为16.9 g-14.9g═2g,
答:剩余固体中氯化钾质量为14.9 g,二氧化锰质量质量为2g.
解答:解:(1)因反应中氧气为气体,则氧气质量为26.5g-16.9g═9.6g,
答:制取氧气的质量为9.6g;
(2)因反应至不再有气体生成,则氯酸钾完全分解,
剩余固体中含氯化钾和二氧化锰,设氯化钾的质量为x,则
2KClO3
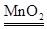 2 KCl+3O2↑
2 KCl+3O2↑149 96
x 9.6g
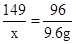 解得x=14.9 g,
解得x=14.9 g,即氯化钾的质量为14.9g,
则二氧化锰质量为16.9 g-14.9g═2g,
答:剩余固体中氯化钾质量为14.9 g,二氧化锰质量质量为2g.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

 (1)在人体中,碘是属于 ▲ (选填“常量”或“微量”)元素。
(1)在人体中,碘是属于 ▲ (选填“常量”或“微量”)元素。
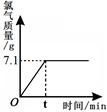
 Cl2↑+ H2↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠恰好完全反应时,得到51.2 g溶液,生成氯气的质量与时间的关系如图所示。请计算:
Cl2↑+ H2↑+ 2NaOH。现取一定质量的氯化钠溶液进行电解,当氯化钠恰好完全反应时,得到51.2 g溶液,生成氯气的质量与时间的关系如图所示。请计算: