题目内容
【题目】研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的过程:
(假设)H2O2生成O2的快慢与催化剂种类有关。
(实验方案)常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间。
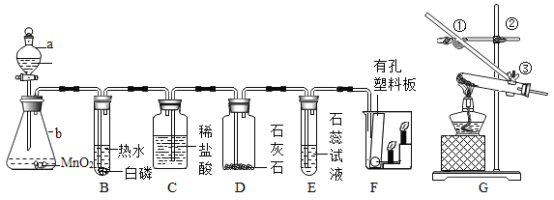
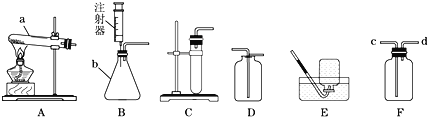
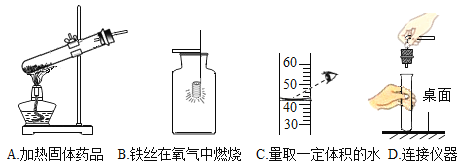
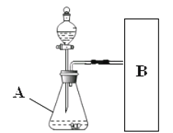
(进行实验)下图是他们进行实验的装置图,气体发生装置中A仪器的名称是(1)_________,此实验中B处宜采用的气体收集方法是(2)_________。
(实验记录)
实验编号 | 1 | 2 |
反应物 | 5%H2O2 | 5%H2O2 |
催化剂 | 1g水泥块 | 1gMnO2 |
时间 | 165s | 46s |
(结论)该探究过程得出的结论是(3)_____________。
(反思)H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快。若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的(4)______和(5)______是否改变。
(实验拓展)H2O2生成O2的快慢还与哪些因素有关?研究性学习小组进行了更深入的探究:
探究实验一:浓度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
取一支试管加入5mL 5%的过氧化氢溶液,然后加入等量的二氧化锰。 | 缓慢有少量气泡冒出 | (6)___________ |
另取一支试管加入5mL 15%的过氧化氢溶液,然后加入等量的二氧化锰。 | 迅速有大量气泡冒出 |
请你设计:
实验用品:试管、烧杯、热水、冷水、5%过氧化氢溶液、15%过氧化氢溶液
探究实验二:温度对化学反应速率的影响
实验步骤 | 现 象 | 结 论 |
取一支试管加入5mL 15%的过氧化氢溶液,把试管放入盛有冷水的烧杯中 | (9)______ | 温度越高,过氧化氢分解的速率越大 |
取一支试管加入5mL(7)___ 的过氧化氢溶液,把试管放入盛有(8)___ 的烧杯中 | (10)______ |
【答案】锥形瓶 排水法或向上排空气法 相同条件下H2O2生成O2的快慢与催化剂的种类有关 质量 化学性质 浓度越大,过氧化氢分解的速率越快 缓慢有少量气泡冒出 15% 热水 迅速有大量气泡冒出
【解析】
[进行实验]气体发生装置中A仪器的名称是锥形瓶;过氧化氢溶液和二氧化锰混合生成水和氧气,氧气不易溶于水,且密度比空气大,因此可以采用排水法或向上排空气法收集;故填:锥形瓶;排水法或向上排空气法;
[结论]
根据控制变量法,分析表中的有关数据,可知分别用1g水泥块和1gMnO2做催化剂,来催化反应时所用的时间分别是165s和46s;由此可知,用1gMnO2做催化剂要比用1g水泥块做催化剂时,化学反应速率要快.因此,由实验现象可以得出的实验结论是:H2O2生成氧气的快慢与催化剂种类有关.故填:相同条件下H2O2生成O2的快慢与催化剂的种类有关;
[反思]
根据催化剂的概念可知,催化剂能改变化学反应的速率,而本身的质量和化学性质在反应前后不改变.故填:质量;化学性质;
探究实验一、根据实验现象可以看出,过氧化氢溶液的浓度越大,在放入二氧化锰时反应越迅速,说明浓度越大,过氧化氢分解的速率越快;故答案为:浓度越大,过氧化氢分解的速率越快;
探究实验二、要探究温度对化学反应速率的影响,由固定变量可知,该实验操作是用试管取一定体积和一定浓度的过氧化氢溶液,分别放入盛放冷水和热水的烧杯中观察发生的现象,放入冷水中的过氧化氢反应不剧烈,而放入热水中的过氧化氢反应剧烈,有大量气泡出现.所以.实验如下:
实验步骤 | 现象 | 结论 |
取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有冷水的烧杯中 | 缓慢有少量气泡冒出 | 温度越高,过氧化氢分解的速率越大 |
取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有热水的烧杯中 | 迅速有大量气泡冒出 |
故答案为:
实验步骤 | 现象 | 结论 |
取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有冷水的烧杯中 | 缓慢有少量气泡冒出 | 温度越高,过氧化氢分解的速率越大 |
取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有热水的烧杯中 | 迅速有大量气泡冒出 |

【题目】下表是元素周期表的一部分:
周期 族 | IA | 0 | ||||||
一 | 1H 1.008 | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 2He 4.003 |
二 | 3Li 6.941 | 4Be 9.012 | 5B 10.81 | 6C 12.01 | 7N 14.01 | 8O 16.00 | 9F 19.00 | 10Ne 20.18 |
三 | 11Na 22.99 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 | 15P 30.97 | 16S 32.06 | 17Cl 35.45 | 18Ar 39.95 |
(1)12号元素的元素符号为_____;C元素的相对原子质量为_____。
(2)相对原子质量为22.99的元素属于_____(填“金属”或“非金属”);Ne的化学性质_____(填稳定或活泼)。氮原子的最外层电子数为_____。科学家宣布已人工合成了第116号元素,则此元素的核电荷数为_____。
(3)表中不同种元素最本质的区别是_____(填字母)
A 质子数不同 B 相对原子质量不同 C 中子数不同
(4)氧、氯、硫、磷在化学反应中一般易_____电子(填“得”或“失”),钠、铝、钾、钙在化学反应中一般易_____电子(填“得”或“失”)趋向达到相对稳定结构。
(