题目内容
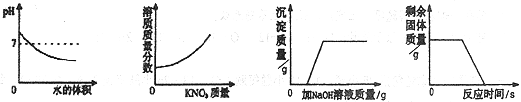
【题目】某兴趣小组测定纯碱样品中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质),取样品13.25g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如图所示,
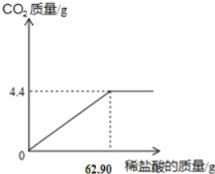
求:
(1)生成二氧化碳的质量为______g;
(2)样品中碳酸钠的质量分数________;
(3)计算恰好完全反应时,所得溶液中溶质的质量分数______________.
【答案】4.4.80%,20%,
【解析】
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据反应的化学方程式和提供的数据可以进行相关方面的计算。
(1)由图中数据可知,生成二氧化碳的质量为4.4g;
(2)解:设样品13.25g中碳酸钠的质量为x,与62.9g稀盐酸恰好完全反应时,生成氯化钠的质量为y,
Na2CO3+2HCl=2NaCl+H2O+CO2↑,
106 117 44
x y 4.4g
![]()
x=10.6g,y=11.7g,
碳酸钠的质量分数为:![]() ×100%=80%,
×100%=80%,
(3)样品中含有的NaCl的质量为:13.25g-10.6g=2.65g,
恰好完全反应时,所得溶液的质量为:13.25g+62.9g-4.4g=71.75g,
恰好安全反应时,所得溶液中溶质的质量分数为:![]() ×100%=20%,
×100%=20%,
答:样品中碳酸钠的质量分数为80%,恰好完全反应时,所得溶液中溶质的质量分数为20%。

 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】某研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧却有明亮的火焰.该小组同学进行如下探究:

(1)探究一:铁丝在氧气中燃烧为什么会火星四射?
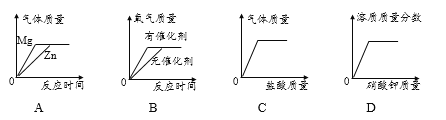
下表是小组同学将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时的现象 | 剧烈燃烧,发出耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
请你分析并回答:写出铁丝在氧气中燃烧的化学表达式:_____,铁燃烧时的“火星四射”现象可能与_____有关,表中未填的一项你估计应当是________。
(2)探究二:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入火焰,导出其中物质,在另一端管口点燃,也有火焰产生.由此可知:蜡烛燃烧产生的火焰是由________(填“固态”或“气态”)物质燃烧构成的。
(3)探究三:物质燃烧产生火焰的根本原因是什么?
查阅资料
物质 | 熔点/℃ | 沸点/℃ | 燃烧时温度/℃ |
石蜡 | 50~70 | 300~550 | 约600 |
铁 | 1535 | 2750 | 约1800 |
钠 | 97.8 | 883 | 约1400 |
由表中数据可知:物质燃烧能否产生火焰与其________(填“熔点”或“沸点”)和燃烧时温度有关,由此推测:钠在燃烧时,________(填“有”或“没有”)火焰产生。