��Ŀ����
����Ŀ��ʵ������һ���Ȼ��ƺ��Ȼ����������Ʒ����ȤС��ͬѧ�������ʵ�鷽�������롢�ᴿ�Ȼ��Ʋ��ⶨ��Ʒ���Ȼ��Ƶ������ٷֺ�������ش��������⣺
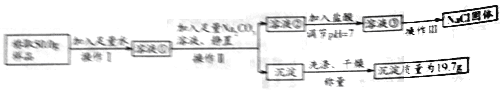
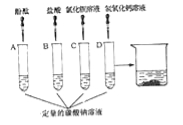
��1����������ƽ������Ʒǰ����ƽ���еĵ�һ��������_________��
��2������Һ���м�������Na2CO3��Һ��Ŀ����___________����С��ͬѧ����ͼ��ʾװ�ý��в���������ָ�������д��ڵ���������________��________________��
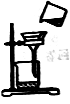
��3�����й��ڲ�������˵����ȷ����___________������ţ���
a���ò������õ��IJ��������оƾ��ơ���������������
b���ò������ò��������Ͻ����Ŀ���Ƿ�ֹ�ֲ��¶ȹ��ߣ����Һ�ηɽ�
c�����������г��ֽ϶����ʱ��ֹͣ����
d��ֹͣ���Ⱥ�������������ֱ�ӷ���ʵ��̨��
��4����Ʒ���Ȼ��������ٷֺ���Ϊ___________��
���𰸡���1��������ƽƽ�⣨1�֣���2��ʹ��Һ�е�BaCl2��ȫ������1�֣� δ�ò�����������1�֣�
©�����¶˹ܿ�δ�����ձ��ڱڣ�1�֣���3��b c��2�֣� ��4��58.4%��2�֣�
����������1��������ƽʹ��ǰ������㣨2��̼���������Ȼ�����Ӧ����̼�ᱵ����������Һ���м�������Na2CO3��Һ��Ŀ���dz��������Ȼ����� ����ע������飺δ�ò��������� ©���¶˹ܿ�δ�����ձ��ڱ� ��3�������ᾧ��ע�����a���ò������õ��IJ��������оƾ��ơ���������������b���ò������ò��������Ͻ����Ŀ����ʹҺ�����Ⱦ��ȣ���ֹ�ֲ��¶ȹ��ߣ����Һ�ηɽ�c������ʱ�����������г��ֽ϶����ʱ����������Һ��ʣ��ʱ��ֹͣ������ ��4���������Ȼ���������Ϊx
BaCl2++Na2CO3=BaCO3��+2NaCl
208 197
x 19.7g
197/19.7g==208/x x=20.8g
�������Ʒ���Ȼ��������ٷֺ���Ϊ58.4%

����Ŀ����ȥ���������к��е��������ʣ������Լ�����ȷ����( )
��� | ����������Ϊ���ʣ� | �����Լ��� |
A | Fe �ۣ�Cu�� | CuSO4 ��Һ |
B | NaCl (ɳ��) | ��ˮ�ܽ⣬���ˡ������ᾧ |
C | Na2SO4 ��Һ�� Na2CO3�� | ����ϡ���� |
D | CO2(CO) | ��ȼ |
����Ŀ��ij��ҵ����(Fe2O3)��Ʒ�п��ܻ���һ�ֺ�ɫ�Ľ������������ʡ����ݹ�ҵ��ȡ��������̷����������ʿ�����FeO��CuO����ȤС��ͬѧΪ̽����Ʒ���Ƿ������ʼ����ʵijɷ֣���������ʵ�顣
��1������ͬѧ�ֱ�ȡ������ȵ���Ʒ��Fe2O3�������Թ��������У�Ȼ���������ϡ���������ͼ����ʵ�飬���ó����ۣ���Ʒ�в������ʡ�����Ϊ�ý���_______����������������������������
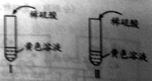
��2������ͬѧ�����в������ʵ�飺
���ռ����ϡ�
�����������������ڼ��������£�������������Ӧ�õ���Ӧ�Ľ������ʺ�ˮ��
����������������Ԫ�ص����������ɴ�С��˳��Ϊ____________��
�������л�������ͭʱ�����Դӽ�����ɫȷ���Ƿ��н���ͭ��
����Ʒ�������ʵ�顿
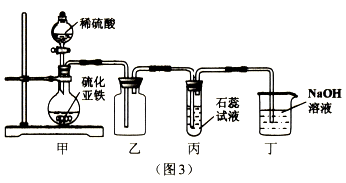
����ͬѧ����ͼװ�ý���ʵ�飨��ʯ�������������������ƹ��������
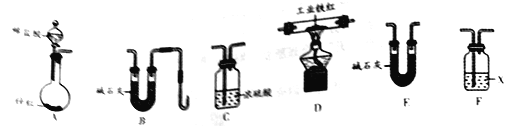
������ͬѧ��ʵ��װ���У��������ӵĺ���˳��ΪA��F��_____��_______��______��B������װ�������Ժ����װ���м���ҩƷ��װ��F���Լ�X��_____��Һ��װ��C��������___________��
������ʵ���������ĺ���˳����________����д������ţ���
a������װ��D�з�Ӧ�� b������H2�Ĵ���
c����װ��A�з�Һ©���Ļ�������Բ����ƿ�м���ϡ����
����ʵ�鴦������ķ�����______________��
��ʵ���������ۡ�
����ͬѧ������ʵ���������±���������ʵ�鹤ҵ�������������ȫ��Ӧ��
ʵ���� | ����װ��D�й�ҵ���������(g) | ʵ���װ��E�����أ�g�� |
1 | 8.0 | 2.6 |
2 | 16.0 | 5.2 |
���������ݣ����ʵ�������_________________��
�����������ͬѧ���ʵ�鷽��ȷ�ϸ���Ʒ�����ʵijɷ�________________����д������������ͽ��ۣ�������Ʒ�в������ʱ��ⲻ������
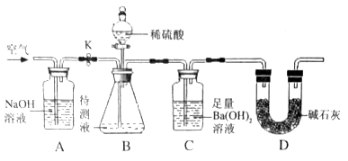
����Ŀ���ڽ��껯ѧʵ��������ԡ�̽����������ʡ��У�ͬѧ��������ͼ��ʾ������ʵ�飬����A��B��C��D��֧�Թ��еķ�Һȫ������һ���ɾ��Ĵ��ձ��У����Խ�����ij��ȤС�鷢�ִ��ձ��ײ��г������ϲ���Һ�ʺ�ɫ��Ϊ��̽���ϲ���Һ�ijɷ֣�����������ʵ�飮
��������⡿���ձ��е��ϲ���Һ�г��˺���ˮ�ͷ�̪�⣬��������Щ���ӣ��������������ʡ�ˮ�ͷ�̪�������������ӣ�
��������衿С����Ϊ�ϲ���Һ��һ������Na+��CO32����H+��Cl����Ba2+��Ca2+��OH���������ӣ�����Ϊ�ϲ���Һ�к��е������������м��֣����Ƿֱ��� �������ӷ��ţ���
���������ۡ���1��С����Ϊ�ϲ���Һ��һ��������H+����Ϊ�ϲ���Һ�ʺ�ɫ����������ϲ���Һ�в�����H+������һ������ ��
��2��С��ȡһ�������ϲ���Һ���Թ��У��μӼ���ϡ���ᣬ���������ݲ�������Ϊ�ϲ���Һ��һ��������CO32����С����Ϊ���Ľ��۲���ȷ��ԭ���� ��
�����ʵ�顿Ϊ��һ��ȷ���ϲ���Һ���Ƿ���CO32���������С��һ���������̽����
ʵ����� | ʵ������ | ʵ����� |
ȡ���ձ����ϲ���Һ������һ֧�Թ��У��μӹ�����BaCl2��Һ������ | �� ���Թ��� ���ϲ���Һ���Ǻ�ɫ | �� ���ձ����ϲ���Һ��һ������CO32�� �� ͬʱ���ܵó����ձ��е��ϲ���Һ��һ������������ �������ӷ��ţ� |
��ʵ����ۡ����ձ��е��ϲ���Һ��һ�����е������� �������ӷ��ţ�