题目内容
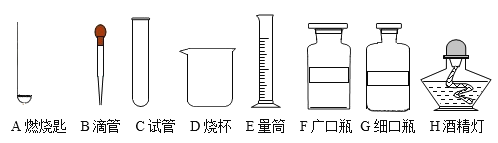
【题目】如图是实验室测定空气中氧气含量实验的装置图:
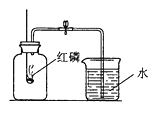
(1)这个实验过程中,下图能正确表示集气瓶内气体体积变化情况的是________。

(2)在此实验过程中能否用蜡烛代替红磷?________(填“能”或“不能”)。请简述理由________。
(3)某活动小组对收集到的气体中氧气的含量产生兴趣。于是将收集到的一瓶氧气密封。
(提出问题)这瓶气体中氧气的体积分数是多少?
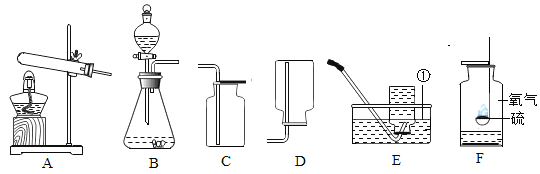
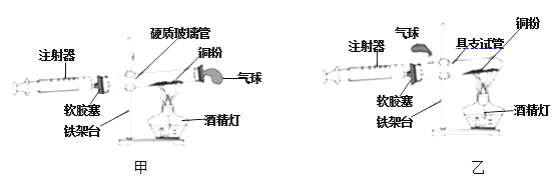
(实验验证)活动小组设计了以下两套实验装置,用来测定该瓶气体中氧气的体积分数:在氮气环境下。将过量的铜粉分别装入干燥的硬质玻璃管和具支试管后,密封。用两支干燥的注射器从该瓶中抽取气体,分别按下图连接,推拉注射器一段时间后,用酒精灯在铜粉部位加热,加热时反复推拉注射器至反应完全。
①甲装置比乙装置更合理,理由是________。
②用甲装置测定氧气的体积分数,需要测定的实验数据是________。
(4)(反思交流)实验完毕,待装置冷却至室温后,应先将气球内的气体全部挤出,再读数。否则会使测得的实验结果________(填“偏大”偏小”或“无影响”),原因是________。
【答案】B 不能 蜡烛燃烧会产生二氧化碳气体,集气瓶内压强减少不明显。 甲装置的气体进入气球时会经过铜粉,使气体与铜粉充分接触,使反应更充分。 实验前后注射器的读数 偏大 气球内含有气体时,会导致反应后读取的注射器读数偏大,从而导致结果偏大。
【解析】
(1)空气中氧气约占五分之一体积,所以红磷燃烧过程中,消耗掉氧气,使得气体的体积减少五分之一,故B图像正确;
(2)蜡烛燃烧生成二氧化碳气体,使压强没有明显变化,所以不能用蜡烛代替红磷;
(3)甲装置的气体进入气球时会经过铜粉,使气体与铜粉充分接触,使反应更充分,而乙装置气体可能直接进入气球,与铜不能充分接触,所以甲装置比乙装置更合理,用甲装置测定氧气的体积分数,需要测定的实验数据是实验前后注射器的读数;
(4)实验完毕,待装置冷却至室温后,应先将气球内的气体全部挤出,再读数,否则气球内含有气体时,会导致反应后读取的注射器读数偏大,从而导致结果偏大。

【题目】某兴趣小组同学对实验室制备氧气的条件进行如下探究实验。
①为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验: Ⅰ.将 3.0g KClO3 与 1.0g MnO2 均匀混合加热
Ⅱ.将 x g KClO3 与 1.0g CuO 均匀混合加热 在相同温度下,比较两组实验产生 O2 的快慢。 Ⅰ中反应的文字表达式是___;
Ⅱ中 x 的值应为___。
②乙探究了影响过氧化氢分解速度的某种因素。实验数据记录如下:
过氧化氢的质量 | 过氧化氢的浓度 | MnO2 的质量 | 相同时间内产生 O2 体积 | |
Ⅰ | 50.0g | 1% | 0.1g | 9mL |
Ⅱ | 50.0g | 2% | 0.1g | 16mL |
Ⅲ | 50.0g | 4% | 0.1g | 31mL |
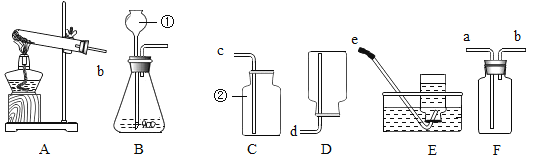
本实验中,测量 O2 体积的装置是___(填编号)。
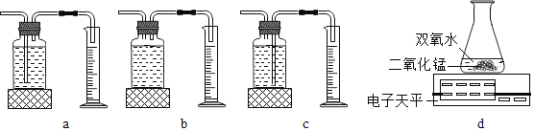
实验结论:在相同条件下,___,过氧化氢分解得越快。 丙用 d 图装置进行实验,通过比较_____也能达到实验目的。
【题目】长期放置于空气中的铜,表面有绿色的物质生成,兴趣小组同学对绿色物质的成分进行下列探究。
(提出问题)绿色物质的成分是什么?
(猜想假设)猜想①:CuO; 猜想②:Cu(OH)2; 猜想③:CuCO3
(讨论交流)同学们做出以上猪想的理论依据是_____;有同学认为猜想①是错误的,其理由是_____。
(查找资料)Cu(OH)2、CuCO3受热易分解,生成物都是氧化物;无水硫酸铜遇水变蓝色。
(实验探究1)
实验 | 实验步骤 | 实验现象 | 实验结论 |
Ⅰ | 取绿色物质于试管中,加入_____,将生成的气体通入澄清石灰水中 | 有气泡产生,生成的气体使澄清石灰水变浑浊 | 猜想_____(填序号)正确 |
Ⅱ | 如下图所示,加热绿色固体 | B中_____ | 猜想②正确 |
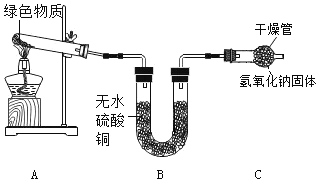
(谈论交流)绿色物质的成分是Cu(OH)2和CuCO3的混合物吗?经询问老师得知绿色物质的成分是 mCu(OH)2 ·nCuCO3.
(实验探究2)取17.3g绿色物质进行反应,经过测定知实验Ⅰ中生成气体的质量为4.4g,实验Ⅱ中装置B的质量曾加0.9 g(假设生成的物质全部被吸收),则m :n=_____ ,
(反思交流)实验Ⅱ中装置C的作用是_____。