题目内容
【题目】实验室常用加热氯酸钾与二氧化锰混合物的方法制取氧气,写出该反应的文字表达式:_____。
小芳发现,氯酸钾与氧化铜或氧化铁混合加热,也能较快产生氧气,于是进行了如下探究:
(提出猜想)除MnO2外,CuO和Fe2O3也可以作KClO3分解的催化剂。
(完成实验)按下表进行实验:测定分解温度(分解温度越低,催化效果越好)。

(得出结论)(1)由实验_____与实验③④对比,可说明猜想合理。
(2)实验所用的三种金属氧化物,催化效果最好的是_____。
(反思)(3)若要证明CuO和Fe2O3是该反应的催化剂,还要验证它们在化学反应前后的质量和____不变。
(4)同种催化剂,颗粒大小可能影响催化效果,请你设计实验方案进行验证:__________
(5)同种催化剂,还有哪些因素可能影响催化效果,请你设计实验探究(探究一种因素即可)。
(影响因素)________。
(实验设计)_____。
【答案】氯酸钾![]() 氯化钾+氧气 ① MnO2 化学性质 将氯酸钾与不同颗粒大小的同种催化剂等质量比充分混合,测定加热分解温度即可 催化剂与反应物的质量比不同,催化效果不同 分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,测定加热分解温度即可
氯化钾+氧气 ① MnO2 化学性质 将氯酸钾与不同颗粒大小的同种催化剂等质量比充分混合,测定加热分解温度即可 催化剂与反应物的质量比不同,催化效果不同 分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,测定加热分解温度即可
【解析】
根据反应物、生成物和条件书写表达式
(1)根据对照试验要求只有一个变量,其他条件都相同进行分析回答;
(2)根据分解温度越低,催化效果越好,结合表中数据进行分析解答;
(3)根据催化剂的定义进行分析回答;
(4)根据对照试验只有一个变量,这个变量为催化剂的颗粒大小设计对照试验;
(5)根据科学探究的环节探究催化剂质量的影响分析。
氯酸钾在二氧化锰催化下加热生成氯化钾和氧气,文字表达式为:氯酸钾![]() 氯化钾+氧气;
氯化钾+氧气;
(1)根据催化剂能改变化学反应的速率,可选择加催化剂和不加催化剂的进行比较分解温度即可,要想证明除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂,可选择实验①和实验④对比,要想证明除MnO2、Fe2O3外,CuO也可以作KClO3分解的催化剂,可选择实验①和实验③对比,证明猜想合理;
(2)分解时所需温度最低的,催化效果越好,分析表中实验数据可以知道MnO2的催化效果最好;
(3)催化剂是指在化学反应里能改变其他物质的化学反应速率(既能提高也能降低),而本身的质量和化学性质在化学反应前后都没有发生改变的物质。故要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的质量和化学性质不变;
(4)要想证明颗粒大小会影响催化效果,可将氯酸钾与不同颗粒大小的同种催化剂等质量比充分混合,测定加热分解温度即可;
(5)催化剂与反应物的质量比不同,催化效果不同;分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,测定加热分解温度即可。

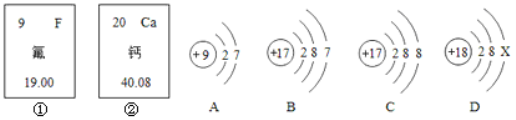
【题目】(1)分类是学习化学常用的方法。
初中化学有许多实验,有的实验侧重于观察和描述,属于观察和描述型实验;有的实验侧重于对一个问题采用控制变量的方法系统探究,属于问题探究型实验。据此可将实验B与实验①_____归为一类。分类的依据是:②___________________________。
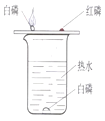
蜡烛及其燃烧的探究 |
探究可燃物燃烧的条件 |
酸、碱与指示剂作用 |
铁制品锈蚀的条件 |
A | B | C | D |
(2)在九年化学书附录I部分,酸、碱、盐的溶解性表中,有些物质溶解性用“—”表示,说明该物质不存在或遇到水就会发生“水解”反应。
例如碳酸铝遇水就会发生“水解”反应:Al 2(CO3)3+ 3H2O==2Al(OH)3↓ + 3CO2↑,据此信息请同学们写出碳酸铁(其中铁元素的化合价与碳酸铝中铝元素的化合价相同)“水解”反应的化学方程式①____________________________,反应过程中观察到的实验现象有②__________________________(答两点)。
【题目】小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:
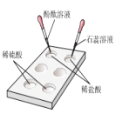
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
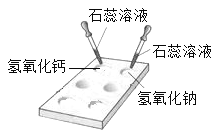
氢氧化钠溶液 | 氢氧化钙溶液 | |
加紫色石蕊溶液 | _______ | ________ |
回忆检验二氧化碳气体的反应,写出该反应的化学方程式:______。
二氧化硫(SO2)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式_____,根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质。(任写两点________、________
(2)如图是某试剂瓶标签上的内容.要把10g这种浓硫酸稀释为20%的硫酸,需要水的质量为______g.量取浓硫酸时仰视读数,会导致结果____________(偏大、偏小)。