题目内容
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。如图是某化学反应的微观过程示意图,请回答相关问题。

(1)A中物质的化学式分别是:______________。
(2)请在B框内将相关粒子的图形补充完整:______。
(3)如图所示反应的化学方程式为:______该反应的生成物所属类别是:________。
(4)如图是氟元素和钙元素在周期表中提供的信息,A、B、C、D为四种粒子的结构示意图,请据图回答下列问题
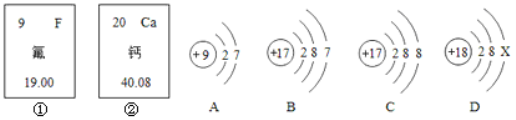
①D原子的结构示意图中x的数值是______。
②图A、B、C、D中,化学性质相似的原子是______。
③氟和钙两种元素最本质的区别是它们原子中的______不同。
④原子序数为17的元素位于元素周期表中第______周期,它属于______(填“金属”或“非金属”)元素;在化学反应中,容易______(填“得到”或“失去”)电子,所形成的粒子的符号是______。
【答案】C 、O2 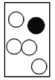 O2+C
O2+C ![]() CO2 氧化物 8 A、B 质子数 3 非金属 得到 Cl-
CO2 氧化物 8 A、B 质子数 3 非金属 得到 Cl-
【解析】
(1)根据某化学反应的微观示意图,由图可知,A中的物质是碳和氧气,化学分别是:C、O2;
(2)根据反应前后原子种类和数目不变,B框内将相关粒子的图形为: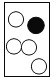 ;
;
(3)如图所示反应是碳和氧气反应生成了二氧化碳,化学方程式为O2+C ![]() CO2;反应的生成物是二氧化碳,二氧化碳是由两种元素组成,其中一种是氧元素,所属类别是氧化物;
CO2;反应的生成物是二氧化碳,二氧化碳是由两种元素组成,其中一种是氧元素,所属类别是氧化物;
(4)①在原子中,核电荷数=质子数=核外电子数,故X=18-2-8=8;
②最外层电子数相同的粒子具有相似的化学性质.A粒子的最外层电子数为7,与其相同的是B,而D图示由原子结构的特点可知X是8,所以A、B的化学性质相同;
③元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数)氟和钙两种元素最本质的区别是它们原子中的质子不同;
④原子序数为17的元素,是氯元素,其原子核外共有3个电子层,位于元素周期表中第三周期,它属于非金属元素;氯原子的最外层电子数为7,大于4,在化学反应中易得到1个电子而形成带1个单位符号的阴离子,所形成的粒子的符号是Cl-。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案【题目】兴趣小组的同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质利用数字化传感器测得烧杯中溶液pH的变化图象进行相关探究。
(提出问题)它们溶液的酸碱性及与酸反应时溶液的pH如何变化?
(实验探究1)向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液(A) | 碳酸钠溶液(B) | 氢氧化钠溶液(C) |
紫甘蓝汁液显示的颜色 | 蓝紫色 | 蓝色 | 绿色 | 黄色 |
查阅资料:
pH | 7.5~9 | 10~11.9 | 12~14 |
紫甘蓝汁液显示的颜色 | 蓝色 | 绿色 | 黄色 |
(得出结论1)三种溶液的碱性由强到弱的顺序为______。(用A、B、C表示)
(实验探究2)甲同学在烧杯溶液中加入约5mL稀氢氧化钠溶液,滴入几滴酚酞溶液,此时溶液由_____色变为____色。向其中加入稀盐酸,该反应的化学方程式为______。
乙同学向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,得到pH变化与时间的关系如下图所示.
(得出结论2)①从微观角度分析,该反应的实质是____。
②如图所示,下列说法正确的是(___________)
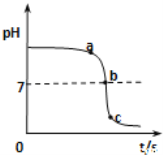
A.图中c点所示溶液呈碱性
B.图中a点所示溶液中,含有的溶质是只有NaCl
C.该实验是将氢氧化钠溶液逐滴滴入到盛有盐酸的烧杯中
D.由a点到b点的pH变化过程证明酸和碱发生了中和反应
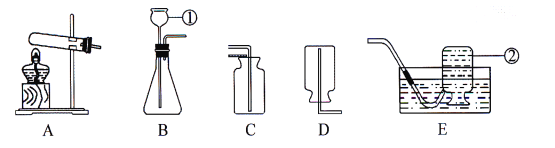
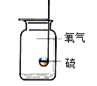
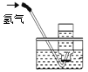
【题目】对下列实验指定容器中的水,其解释没有体现水的主要作用的是
A | B | C | D | |
实 验 装 置 |
|
硫在氧气中燃烧 |
铁丝在氧气中燃烧 |
排水法收集氢气 |
解 释 | 量筒中的水:通过水体积的变化得出的氧气体积 | 集气瓶中的水:吸收放出的热量。 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶内的空气排净,后便于观察氢气何时收集满 |
A. A B. B C. C D. D