题目内容
【题目】氢氧化钙和氢氧化钠是两种常见的碱。小花同学将两种碱溶液分别装入试管A、B两支试管中,并进行如下图所示的三组实验。

(1)实验1中,两支试管的溶液都变成________色。
(2)实验2中,若试管B中盛装的是NaOH溶液,发生反应的化学方程式为___________________________,该反应的基本类型是_______反应。
(3)实验3中,某同学向两支试管中吹气,A中有白色沉淀产生,发生反应的化学方程式为______________________________。B中无明显现象,为了探究吹气后B中溶质的成分,该同学进行了如下探究。
(提出猜想)猜想1:溶质是氢氧化钠;
猜想2:溶质是碳酸钠;
猜想3:溶质是_____________。
溶质中出现碳酸钠的原因是氢氧化钠与__________发生了反应。
(实验和结论)
实验 | 实验现象 | 结论 |
取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,静置后取上层清液,向其中滴加几滴酚酞溶液 | ____________ | 猜想3成立 |
(反思与评价)
老师评价该同学得出的结论不正确,是因为猜想2也会产生相同的现象。如果要验证“猜想3成立”,必须要将氢氧化钙溶液换成_________溶液。
【答案】 红 2NaOH + CuSO4 == Na2SO4 + Cu(OH)2↓ ; 复分解 Ca(OH)2 + CO2 == CaCO3↓+ H2O 氢氧化钠和碳酸钠; 二氧化碳 产生白色沉淀无色酚酞溶液变红 氯化钙(合理即可)
【解析】本题考查了实验探究物质的组成,碱、盐的化学性质。认真审题,根据题给出信息,结合已有的知识进行分析解答。
(1)实验1中,两支试管的溶液都显碱性,都能够使酚酞试液变红色;
(2)实验2中,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式是2NaOH + CuSO4 == Na2SO4 + Cu(OH)2↓;该反应是由两种化合物互相交换成分,生成另外两种化合物的反应,属于复分解反应;
(3)实验3中,向两支试管吹气,A中有白色沉淀生成,说明A中是澄清石灰水,澄清石灰水中的氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,发生反应的化学方程式为:Ca(OH)2 + CO2 == CaCO3↓+ H2O;
提出猜想:氢氧化钠与二氧化碳反应生成碳酸钠和水,当恰好完全反应时,所得溶液中的溶质是碳酸钠,当吹入二氧化碳量少时,所得溶液的溶质是氢氧化钠和碳酸钠。所以猜想3:溶质是氢氧化钠和碳酸钠;溶质中出现碳酸钠的原因是氢氧化钠与二氧化碳发生了反应;
实验和结论:若猜想3成立,溶液中存在氢氧化钠和碳酸钠,碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,加入澄清石灰水后,产生白色沉淀,加入澄清石灰水至不再产生沉淀为止,静置后取上层清液,上层清液中存在氢氧化钠,氢氧化钠溶液呈碱性,能使无色的酚酞变红色,所以向其中滴加几滴酚酞溶液,溶液变红色,因此:
实验 | 实验现象 | 结论 |
取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,静置后取上层清液,向其中滴加几滴酚酞溶液 | 产生白色沉淀无色酚酞溶液变红 | 猜想3成立 |
反思与评价:如果要验证“猜想3成立”,必需更换试剂,将氢氧化钙溶液换成氯化钙溶液,这是因为氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,氯化钠溶液显中性,不能使酚酞试液变色。取B中少量溶液,加入氯化钙溶液至不再产生沉淀为止,静置后取上层清液,向其中滴加几滴酚酞溶液,若产生白色沉淀,说明溶液中存在碳酸钠,无色酚酞溶液变红,说明溶液中存在氢氧化钠。

 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案【题目】实验小组同学通过以下实验研究二氧化碳的性质。
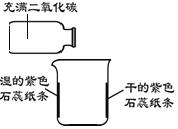
| ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的集气瓶轻轻在烧杯上方倾斜 | 一段时间后,湿的紫色石蕊纸条变为红色 |
(1)烧杯内壁上贴干的紫色石蕊纸条的目的是__________。
(2)该实验发生反应的化学方程式为__________。