题目内容
【题目】实验小组同学通过以下实验研究二氧化碳的性质。
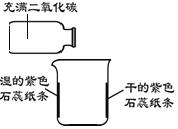
| ①在烧杯内壁上贴上干的和用水润湿的紫色石蕊纸条 ②将充满二氧化碳的集气瓶轻轻在烧杯上方倾斜 | 一段时间后,湿的紫色石蕊纸条变为红色 |
(1)烧杯内壁上贴干的紫色石蕊纸条的目的是__________。
(2)该实验发生反应的化学方程式为__________。
【答案】 证明二氧化碳不能使干燥的紫色石蕊变红 H2O + CO2 ![]() H2CO3
H2CO3
【解析】本题考查了二氧化碳和水反应的实验。
(1)通过对照实验,一段时间后,湿的紫色石蕊纸条变为红色,干的紫色石蕊纸条没有就色,烧杯内壁上贴上干的紫色石蕊纸条的目的是证明二氧化碳不能使干燥的紫色石蕊变红;
(2)二氧化碳与水反应生成碳酸,碳酸呈酸性,能使紫色石蕊变红。该实验发生反应的化学方程式为H2O + CO2 ![]() H2CO3。
H2CO3。

【题目】为探究酸、碱、盐的化学性质,某兴趣小组做了如下实验。

试回答下列问题
(1)试管A中的现象是______________________。
(2)试管B中反应的化学方程式为_____________________________。
(3)甲同学把反应后的C、D试管中的废液倒入一只洁净的烧杯中,观察到先有气泡产生,后有白色沉淀生成;过滤后得到白色沉淀和无色滤液。甲同学欲探究无色滤液中溶质的成分。
(提出问题)无色滤液中的溶质是什么?
(作出猜想)
猜想I NaCl
猜想I I NaCl和CaCl2
猜想Ⅲ NaCl 和Na2CO3
猜想IV:NaCl 、CaCl2 和Na2CO3
小明认为猜想IV定不成立,其原因是____________________(用化学方程式表示)。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
i.取少量滤液于试管中,滴加少量碳酸钠溶液 | 无明显现象 | 猜想____成立 |
ⅱ.取少量滤液于试管中,滴加少量____ | 有气泡产生 |
【题目】某兴趣小組为测定石灰石中碳酸钙的质量分数,取12g石灰石样品加入烧杯中,将120g稀盐酸平均分四次加入,充分反应后(杂质不溶于水也不与稀盐酸反应),测得实验数据如下:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸的质量/g | 30 | 30 | 30 | 30 |
剩余固体的质量/g | 9 | 6 | 3 | 2 |
分析数据计算(結果精确到0.1%):
(1)该祥品中碳酸钙的质量分数为__________。
(2)所用稀盐酸的溶质质量分数为__________。
(3)12g样品中的碳酸钙恰好完全反应时所得溶液的溶质质量分数为__________。
【题目】氢氧化钙和氢氧化钠是两种常见的碱。小花同学将两种碱溶液分别装入试管A、B两支试管中,并进行如下图所示的三组实验。

(1)实验1中,两支试管的溶液都变成________色。
(2)实验2中,若试管B中盛装的是NaOH溶液,发生反应的化学方程式为___________________________,该反应的基本类型是_______反应。
(3)实验3中,某同学向两支试管中吹气,A中有白色沉淀产生,发生反应的化学方程式为______________________________。B中无明显现象,为了探究吹气后B中溶质的成分,该同学进行了如下探究。
(提出猜想)猜想1:溶质是氢氧化钠;
猜想2:溶质是碳酸钠;
猜想3:溶质是_____________。
溶质中出现碳酸钠的原因是氢氧化钠与__________发生了反应。
(实验和结论)
实验 | 实验现象 | 结论 |
取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,静置后取上层清液,向其中滴加几滴酚酞溶液 | ____________ | 猜想3成立 |
(反思与评价)
老师评价该同学得出的结论不正确,是因为猜想2也会产生相同的现象。如果要验证“猜想3成立”,必须要将氢氧化钙溶液换成_________溶液。