题目内容
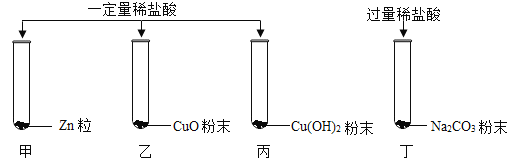
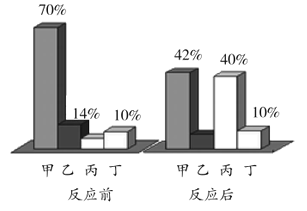
【题目】在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是
A.丙一定是化合物
B.反应后乙的质量分数是10%
C.丁一定是该反应的催化剂
D.该反应是分解反应
【答案】A
【解析】
反应前丙的质量分数是:1-70%-14%-10%=6%,反应后乙的质量分数是:1-42%-40%-10%=8%,分析反应前后各物质质量分数可知,甲和乙为反应物,丙为生成物,丁为催化剂或不反应的杂质,即该反应为化合反应。
A、根据分析知,甲、乙是反应物,丙是生成物,丁是催化剂或杂质,则丙一定是化合物,故A正确;
B、反应后乙的质量分数是:1-42%-40%-10%=8%,故B错误;
C、丁可能是该反应的催化剂,也可能是杂质,故C错误;
D、根据分析知,该反应是化合反应,故D错误。
故选A。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案【题目】氢化钙(CaH2)是一种白色细颗粒状固体,能与水发生剧烈反应,其反应的化学方程式为:![]() ,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是_____。为进一步确定滤液中所含溶质的成分,他们进行了以下实验探究。
,常用作登山运动员的能源提供剂。某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是_____。为进一步确定滤液中所含溶质的成分,他们进行了以下实验探究。
[提出猜想]猜想一: NaOH
猜想二: NaOH 和Ca(OH)2
猜想三: NaOH、Na2CO3
猜想四: NaOH、 Na2CO3、 Ca(OH)2
经过讨论,大家一致认为猜想四不合理,理由是(用化学方程式表示)______。
[实验验证]
实验 | 现象 | 结论 |
(1)取少量滤液,向其中滴入少量碳酸钠溶液 | 无明显现象 | 猜想___不成立 |
(2)另取少量滤液,向其中加入______ | _____ | 猜想三成立 |
[反思与拓展]若向NH4Cl的溶液中加入一定量的CaH2,充分反应,产生的气体有氢气和___。