题目内容
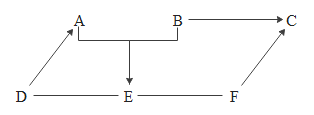
【题目】A、B、C、D、E、F 是初中化学常见的六种物质,其中 A 和 E 都是酸,B、D 只含两种元素,C 是一种不溶于稀硝酸的白色沉淀,而 C、D、F 是与 A、E 不同的三类化合物,它们之间的关系如图所示,“→”表示物质间的转化关系,“一”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出)。
请回答:
(1)A 的化学式__________
(2)写出 F→C 反应的化学方程式 ___________
【答案】H2SO4 H2SO4+Ba(OH)2=BaSO4 ↓+2H2O
【解析】
根据题意可知, A 和 E 都是酸,A 与 B反应生成E,A为硫酸,E为盐酸,则B为氯化钡;A 和 D 能反应, D 只含两种元素, 因此D为金属氧化物;由图可知 B能转化为C,C 是一种不溶于稀硝酸的白色沉淀,故C 是硫酸钡或氯化银, E与F能反应,F能转化为C,且F 是与 A、E 不同的三类化合物,所以F 是氢氧化钡,则C是硫酸钡,带入验证符合图示规律。
(1)由分析可知,A 的化学式H2SO4,故填写:H2SO4;
(2)由分析可知,F 是氢氧化钡,C 是硫酸钡,F能转化为C,方法是加入稀硫酸,硫酸与氢氧化钡反应生成水和沉淀硫酸钡,故填写:H2SO4+Ba(OH)2=BaSO4 ↓+2H2O。

 阅读快车系列答案
阅读快车系列答案【题目】一同学用某种粗盐进行提纯实验,步骤见下图。

请回答:
(1)步骤①和②的操作名称是 。
(2)步骤③判断加入盐酸“适量”的方法是 ;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止 ,当蒸发皿中有较多量固体出现时,应 ,用余热使水分蒸干。
(3)猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含CaCO3、MgCO3 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 | | 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含BaCO3 | 取少量固体A于试管中,先滴入 ,再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水, | | 猜想Ⅲ成立 |