题目内容
【题目】根据所示的实验或装置,回答问题:
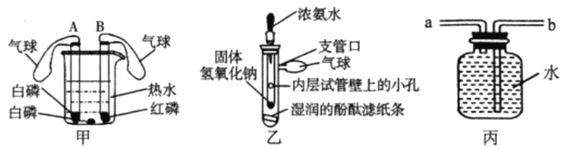
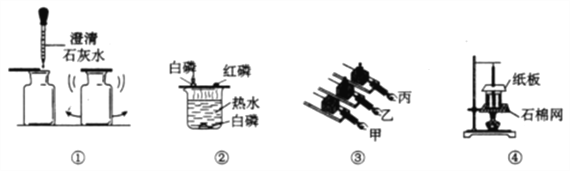
(1)甲实验的目的是:_______________________。
(2)乙实验中,向内层试管内滴入少量浓氨水后,湿润的酚酞滤纸条处出现的现象是_____________。实验中氢氧化钠固体的作用是________________________。
(3)丙装置在化学实验中具有广泛的用途,俗称“万能瓶”,若用该装置收集氧气,气体应从装置的__________端进入(选填“a”或“b”)。
【答案】 探究物质燃烧所需要的条件 纸条变为红色 氢氧化钠吸水放热,加速浓氨水挥发 a
【解析】(1)根据实验中产生的现象分析解答;(2)氨水显碱性,能使酚酞试液变红;氢氧化钠固体具有吸水性,溶于水时放出大量的热;(3) 根据氧气比水的密度小,所以收集的气体在水的上部,利用气体的压力将水排出解答。(1)由甲图可知,A试管内的白磷能燃烧,B试管内的红磷不燃烧,烧杯中的白磷不燃烧可知,甲实验的目的是:探究物质燃烧所需要的条件;(2)乙实验中,向内层试管内滴入少量浓氨水后,湿润的酚酞滤纸条处出现的现象是纸条变为红色;实验中氢氧化钠固体的作用是氢氧化钠吸水放热,加速浓氨水挥发;(3) 氧气比水的密度小,所以收集的气体在水的上部,利用气体的压力将水排出,气体应该是“短进长出”,故选a。

 阅读快车系列答案
阅读快车系列答案【题目】下列实验目的、操作、现象、结论都正确的是
选项 | 实验目的 | 实验操作 | 实验现象 | 实验结论 |
A | 测溶液pH | 用玻璃棒蘸取待测液滴在用蒸馏水润湿的pH试纸上 | 试纸变为浅红色 | 溶液pH为2 |
B | 鉴别NaOH和NH4NO3 | 在装有等量水的试管中分别加入a、b固体 | 加a的试管水温升高,加b的试管水温降低 | a是NaOH b是NH4NO3 |
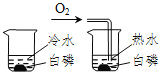
C | 验证燃烧是否需要O2 |
| 前者不燃烧,后者燃烧 | 燃烧需要O2 |
D | 比较Al、Cu的活泼性 | 将未经打磨的Al条放入CuSO4溶液中 | 无明显现象 | 活泼性Al<Cu |
A. A B. B C. C D. D