题目内容
木炭不充分燃烧生成一氧化碳:
2C+O2
2CO
| ||
2C+O2
2CO
.
| ||
分析:木炭不充分燃烧生成一氧化碳,写出反应的化学方程式即可.
解答:解:木炭不充分燃烧生成一氧化碳,反应的化学方程式为:2C+O2
2CO.
故答案为:2C+O2
2CO.
| ||
故答案为:2C+O2
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
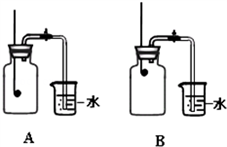
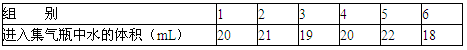
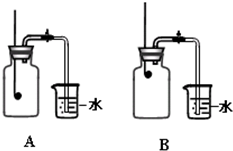 某校化学兴趣小组就空气中氧气的含量进行实验探究:
某校化学兴趣小组就空气中氧气的含量进行实验探究: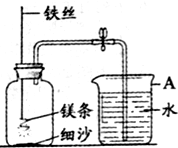 A仪器的名称是
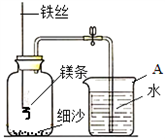
A仪器的名称是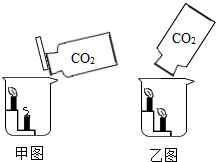 化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.
化学兴趣小组的同学对碳及碳的氧化物进行了一系列拓展性探究学习.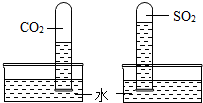
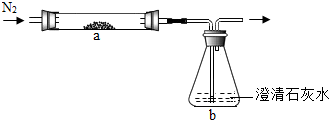
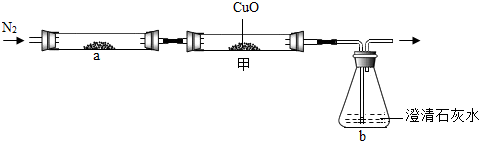
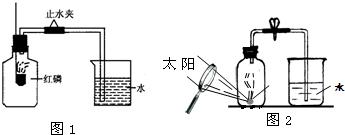
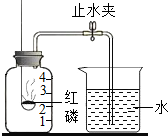 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: