题目内容
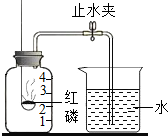 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:①将图中的集气瓶分为5等分,并作好标记.
②在带橡胶塞和导管的燃烧匙内装入足量的红磷;将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡胶塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.请回答下列问题:
(1)该实验中红磷需稍过量,目的是:
确保集气瓶内的氧气消耗尽
确保集气瓶内的氧气消耗尽
.(2)步骤③中打开止水夹后观察到的现象是
烧杯中的水倒流至集气瓶,液面上升在一等分刻度处
烧杯中的水倒流至集气瓶,液面上升在一等分刻度处
,由此可得出空气中氧气的体积约为五分之一
五分之一
.(3)写出红磷燃烧的化学方程式:
4P+5O2
2P2O5
| ||
4P+5O2
2P2O5
.
| ||
(4)写出碳燃烧的化学方程式:
C+O2
CO2
| ||
C+O2
CO2
,结合化学方程式回答能否用木炭代替红磷完成上述探究实验:
| ||
不可以
不可以
(填“可以”或“不可以”),原因是木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化
木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化
.分析:(1)根据该实验注意事项分析;
(2)根据红磷的燃烧结合压强知识分析,红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶;根据实验现象分析;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(4)根据化学方程式的书写方法、步骤进行书写即可;根据木炭燃烧的产物结合压强知识进行解答.
(2)根据红磷的燃烧结合压强知识分析,红磷与氧气反应生成固体,消耗了瓶内的气体,压强减小,外界大气压会压着水进入集气瓶;根据实验现象分析;
(3)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
(4)根据化学方程式的书写方法、步骤进行书写即可;根据木炭燃烧的产物结合压强知识进行解答.
解答:解:(1)实验的目的是测定空气中氧气含量,原理是消耗氧气使装置内外产生压强差,水被吸入占据氧气的空间,从而达到测定氧气的目的,红磷过量,可使集气瓶中的氧气完全消耗;
(2)红磷与氧气反应,生成了五氧化二磷固体,所以会导致集气瓶内压强减小,水被压入集气瓶,进入的水量正好占据集气瓶内氧气的空间,约为集气瓶体积的五分之一;据实验现象可得出空气中氧气的体积分数约为五分之一;
(3)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2
2P2O5;
(4)碳在氧气中燃烧生成了二氧化碳,故可以写出该反应的化学方程式:C+O2
CO2;木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化,所以实验失败;
故答案为:(1)确保集气瓶内的氧气消耗尽;
(2)烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;五分之一;
(3)4P+5O2
2P2O5;
(4)C+O2
CO2;木炭燃烧生成了二氧化碳气体,不能使瓶中压强出现明显的变化.
(2)红磷与氧气反应,生成了五氧化二磷固体,所以会导致集气瓶内压强减小,水被压入集气瓶,进入的水量正好占据集气瓶内氧气的空间,约为集气瓶体积的五分之一;据实验现象可得出空气中氧气的体积分数约为五分之一;
(3)红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2
| ||
(4)碳在氧气中燃烧生成了二氧化碳,故可以写出该反应的化学方程式:C+O2
| ||
故答案为:(1)确保集气瓶内的氧气消耗尽;
(2)烧杯中的水倒流至集气瓶,液面上升在一等分刻度处;五分之一;
(3)4P+5O2
| ||
(4)C+O2
| ||
点评:熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (2005?崇文区二模)某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
(2005?崇文区二模)某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
 某同学设计了测定空气中氧气含量的实验,实验装置如图所示.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图所示.该同学的实验步骤如下: 某同学设计了测定空气中氧气含量的实验,实验装置如图.
某同学设计了测定空气中氧气含量的实验,实验装置如图.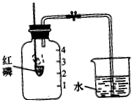 某同学设计了测定空气中氧气含量的实验,装置如图,该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,装置如图,该同学的实验步骤如下: