题目内容
【题目】“第三届国际氢能与燃料电池汽车大会”于2018年10月23日在如皋召开。
Ⅰ.氢燃料电池
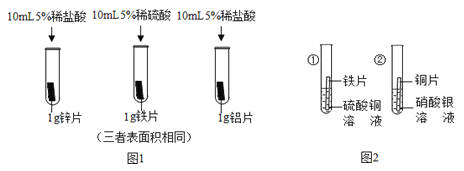
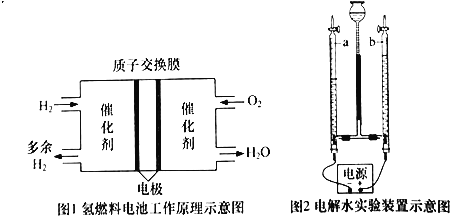
(1)图1所示为氢燃料电池的工作原理:将氢气送到燃料电池中,经过催化剂的作用,通过质子交换膜,再与氧气反应,同时产生电流。请写出氢燃料电池中发生反应的化学方程式:______________________。
Ⅱ.制氢
铁酸锌(ZnFe2O4)可用于循环分解水制取氢气,其中涉及的反应有:
①6ZnFe2O4![]() 6ZnO+ 4Fe3O4+O2↑;
6ZnO+ 4Fe3O4+O2↑;
②3ZnO+2Fe3O4+H2O![]() 3ZnFe2O4+H2↑
3ZnFe2O4+H2↑
(2)ZnFe2O4中Fe的化合价为___________。
(3)该循环制氢中不断消耗的物质是___________,所得H2和O2的质量比为___________。
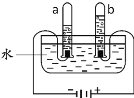
(4)电解水也可制得H2。图2所示装置中,___________(填“a”或“b”)管中产生的气体为氢气
Ⅲ.储氢
(5)在常温和250 kPa下,镧镍合金(LaNi5)吸收氢气生成 LaNi5H7,该物质能在一定条件下分解释放出氢气,该储氢原理属于___________变化。
【答案】2H2+O2![]() 2H2O +3 水(或H2O) 1∶8 a 化学
2H2O +3 水(或H2O) 1∶8 a 化学
【解析】
Ⅰ
(1)由图可知氢气和氧气在催化剂的条件下生成水,故填2H2+O2![]() 2H2O;
2H2O;
Ⅱ
(2)铁酸锌中锌元素化合价是+2,氧元素化合价是-2价 ,根据化合价代数和为零的原则,可知铁酸锌中铁的化合价是+3价,故填+3;
(3)由题中两个循环制氢的化学反应方程式可知不断消耗的物质是水,故填水(或H2O);水中氢氧元素质量比为2∶16=1∶8,所得氢气和氧气的质量比也是1∶8,故填1∶8;
(4)电解水制氢气时,和电源负极相连的是氢气,和电源正极相连的是氧气,且氢气和氧气的体积比是2∶1,故填a;
Ⅲ
(5)镧镍合金(LaNi5)吸收氢气生成 LaNi5H7,属于化学变化,故填化学。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】如图所示,在分别盛有100g水的烧杯中放入KNO3充分溶解,则说法正确的是( )
温度(℃) | t1 | t2 |
KNO3的溶解度(g/100g水) | 60 | 90 |
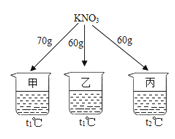
A. 乙、丙溶液中溶质质量相等
B. 乙升温至t2℃,溶液质量增加
C. 甲、乙混合后为t1℃的不饱和溶液
D. 丙降温至t1℃,有晶体析出