题目内容
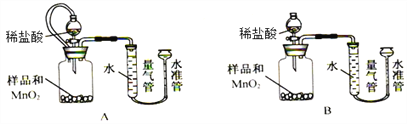
【题目】为了从电路板的废腐蚀液(含有CuCl2、FeCl2和FeCl3)中回收铜,并重新得到FeCl3溶液,设计如下实验流程。(已知:2FeCl3+Fe=3FeCl2)
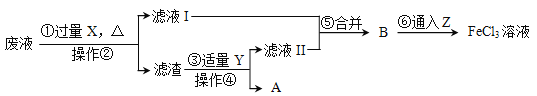
(1)操作②的名称是___________。
(2)上述流程中,X的化学式是______,加入X需过量的原因是____________________。步骤③中发生反应的化学方程式是____________,其基本反应类型是__________。
(3)Z为Cl2,第⑥步发生的反应为化合反应,此反应的化学方程式是________________。
【答案】过滤 Fe 使溶液中的氯化铁、氯化铜完全反应 Fe+2HCl=FeCl2+H2↑ 置换反应 2FeCl2+Cl2=2FeCl3
【解析】
(1)操作②的名称是过滤,通过过滤把液体和不溶于水的固体分离;
(2)上述流程中,铁能和氯化铜反应生成氯化亚铁和铜,铁能和氯化铁反应生成氯化亚铁,所以加入的物质X是铁粉,化学式为:![]() ,加入过量的原因是:使溶液中的氯化铁、氯化铜完全反应,步骤③中,加入的适量的Y是稀盐酸,稀盐酸能和铁反应生成氯化亚铁和氢气,化学方程式为:
,加入过量的原因是:使溶液中的氯化铁、氯化铜完全反应,步骤③中,加入的适量的Y是稀盐酸,稀盐酸能和铁反应生成氯化亚铁和氢气,化学方程式为:![]() ,其基本反应类型是置换反应;
,其基本反应类型是置换反应;
(3)氯化亚铁和氯气反应生成氯化铁,化学方程式为:![]() .
.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2。某研究小组取100 g生氧剂放入装置A中,加入足量水使之充分反应(4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量。他们进行了三次实验,测定结果如下:
测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.0 |
反应后装置A总质量(g) | 376.1 | 376.1 | 375.8 | 376.0 |
请根据上述实验结果计算:(假设杂质不含钾元素且不与水反应)
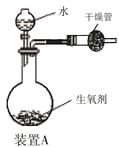
(1)100 g 生氧剂与水反应生成的氧气质量;
(2)生氧剂中含钾元素的质量分数。
【题目】下表是Ca(OH)2和NaOH的溶解度数据。请回答下列问题:
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
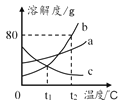
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,如图中能表示NaOH溶解度曲线的是__________(填“A”或“B”)。
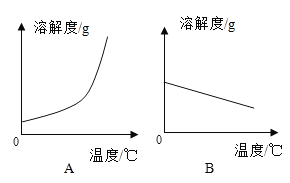
(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,可采取措施有__________(填序号)。
①蒸发水;②升高温度;③降低温度;④加入水;⑤加入氢氧化钙。
(3)现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后恢复20℃,得到乙溶液,溶液中溶质的质量分数的关系为甲________乙(填“>”、“<”或“=”)。