题目内容
【题目】有一种自生氧防毒面具,其使用的生氧剂的主要成分是KO2。某研究小组取100 g生氧剂放入装置A中,加入足量水使之充分反应(4KO2+2H2O=4KOH+3O2↑),测定反应前后装置A的总质量。他们进行了三次实验,测定结果如下:
测定序号 | 第1次 | 第2次 | 第3次 | 平均值 |
反应前装置A总质量(g) | 400.1 | 400.2 | 399.7 | 400.0 |
反应后装置A总质量(g) | 376.1 | 376.1 | 375.8 | 376.0 |
请根据上述实验结果计算:(假设杂质不含钾元素且不与水反应)
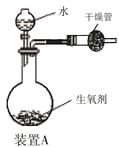
(1)100 g 生氧剂与水反应生成的氧气质量;
(2)生氧剂中含钾元素的质量分数。
【答案】(1)24g
【解析】
试题解:(1)由题意可得,100g生氧剂与水反应生成的氧气质量为400g-376g=24g。
(2)设生氧剂中KO2的质量为x.
4KO2+2H2O=4KOH+3O2↑
284 96
x 24g
![]()
x=71g
生氧剂中钾元素的质量分数:![]() ×100% =39%
×100% =39%
答:(1)100g生氧剂与水反应生成的氧气质量为24g。
(2)该生氧剂中钾元素的质量分数是39%。

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目