题目内容
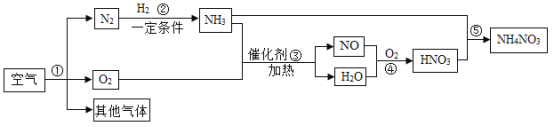
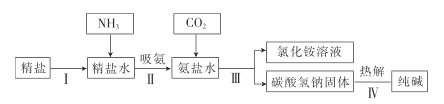
【题目】海洋是人类宝贵的自然资源,如图是利用海水“制碱”的部分流程。请完成下列问题:
(查阅资料)
①在20℃时,1份体积的水可溶解700份体积的氨,溶液显碱性。
②在20℃时,1份体积的水可溶解约1份体积的二氧化碳,二氧化碳溶于水生成碳酸。
(1)步骤Ⅲ的反应原理是著名的“侯氏制碱法”的重要反应,依据质量守恒定律推断反应物是![]() 、____________(填化学式)。
、____________(填化学式)。
(2)步骤Ⅳ发生反应的化学方程式为__________________.
(3)工业上采用氨碱法生产纯碱的工艺是先向饱和食盐水中通人较多的![]() ,再通入足量的
,再通入足量的![]() ,其原因是_______________(填字母)。
,其原因是_______________(填字母)。
A![]() 比
比![]() 更易制取
更易制取
B![]() 的密度比
的密度比![]() 大
大
C使![]() 更易被吸收
更易被吸收
D为了增大![]() 的溶解度
的溶解度
【答案】CO2、H2O、NaCl 2NaHCO3![]() Na2CO3+CO2↑+H2O C
Na2CO3+CO2↑+H2O C
【解析】
(1)步骤三的生成物是氯化铵和碳酸氢钠,反应物中有氨气,依据质量守恒定律推断反应物中含有二氧化碳、水和氯化钠;故填:CO2、H2O、NaCl;
(2)步骤Ⅳ的反应是碳酸氢钠在加热的条件下分解为碳酸钠、水和二氧化碳;故填:2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(3)先向饱和食盐水中通入氨气,制成饱和氨盐水溶液显碱性,再向其中通过二氧化碳,其原因是能够更多、更快的吸收二氧化碳。故填:C。

练习册系列答案
相关题目