题目内容
【题目】已知:Al(OH)3沉淀可溶于NaOH溶液,其反应方程式为:Al(OH)3+NaOH=NaAlO2+2H2O
现向100g HCl和AlCl3的混合溶液中逐滴加入质量分数为20﹪的NaOH溶液,产生沉淀的质量与所加NaOH溶液的质量关系如图所示。回答下列问题:

(1)原混合溶液中HCl的质量分数是______。
(2)当沉淀达到最大值时生成NaCl的质量是_____?
(3)m2=____。
【答案】3.65% 23.4 g 100
【解析】
根据图中数据可以看出和盐酸反应的氢氧化钠溶液的质量为20g;氢氧化钠和氯化铝反应生成的沉淀的质量为7.8g;根据以上数据和对应的化学方程式求算对应的数据。
(1)由图可以看出和盐酸反应的氢氧化钠溶液的质量为20g,其溶质的质量为20%×20g=4g
设混合溶液中HCl的质量为x,生成的氯化钠的质量为y。
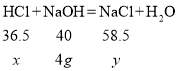
![]()
x=3.65g
y=5.85g
原混合溶液中HCl的质量分数为![]()
(2)由于生成的氢氧化铝的质量为7.8g,设生成的氯化钠的质量为z,消耗的氢氧化钠的质量为a。

![]()
a=12g
z=17.55g
当沉淀达到最大值时生成NaCl的质量是5.85g+17.55g=23.4g
(3)设与氢氧化铝反应需要氢氧化钠的质量为b。
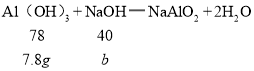
![]()
b=4g
到沉淀完全溶解消耗的氢氧化钠的质量为4g+12g+4g=20g
对应的氢氧化钠溶液的质量为![]() 。
。
答:
(1)原混合溶液中HCl的质量分数是3.65%。
(2)当沉淀达到最大值时生成NaCl的质量是23.4g。
(3)m2=100。

 互动课堂系列答案
互动课堂系列答案【题目】 小明对妈妈杀鱼时从鱼肚内取出的鳔(如图)产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占1/4,其余主要是二氧化碳和氮气.探究分两步进行.
(1)测量鳔内气体体积.小明设计了两种方法:
A:用医用注射器抽取鳔内气体,测量其体积;B:在水下剌破鳔,用排水集气法收集鳔内气体并测量其体积(如图).
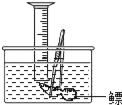
你认为这两种方法中不合理的是_____,理由:_____.写出与理由相关的化学方程式_____.
(2)探究鳔内气体的成分.给你两集气瓶的鳔内气体,请你帮助他设计实验验证假设.
方法 | 现象 | |
验证鳔内含O2 | _____ | _____ |
验证鳔内含CO2 | _____ | _____ |