题目内容
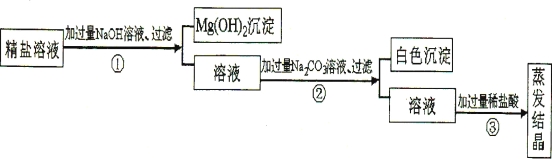
【题目】A﹣J及X均为初中化学所学的物质,它们相互转化的关系如图所示(部分生成物未标出).其中C为常见建筑材料的主要成分,F为蓝色沉淀,H为不溶于稀硝酸的白色沉淀,I和X为常见的金属单质,E为蓝色溶液,J为浅绿色溶液,B、D、E、G、J的溶液中只含一种溶质.
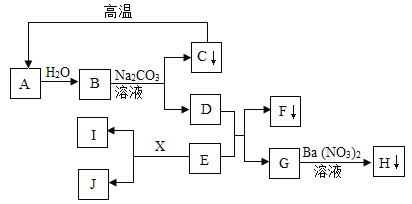
据此,请回答下列问题:
(1)物质H的化学式为_____
(2)写出下列化学方程式:B+Na2CO3→C+D_______________________________。
(3)D+E→F+G的基本反应类型_________________。
【答案】 BaSO4 Ca(OH)2 + Na2CO3 ====CaCO3 ↓ + 2NaOH 复分解反应
【解析】C为常见建筑材料的主要成分,又是沉淀,则C是CaCO3,CaCO3![]() CaO+CO2↑,则A是CaO,CaO+H2O==Ca(OH)2,B是Ca(OH)2,Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH,D是NaOH。F为蓝色沉淀,F是Cu(OH)2,G+Ba(NO3)2→H,H为不溶于稀硝酸的白色沉淀,则H是BaSO4,E是CuSO4。I和X为常见的金属单质,J为浅绿色溶液,则x是Fe,I是Cu,J是FeSO4 。(1)物质H是BaSO4 。(2)B+Na2CO3→C+D的化学方程式为:Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH
CaO+CO2↑,则A是CaO,CaO+H2O==Ca(OH)2,B是Ca(OH)2,Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH,D是NaOH。F为蓝色沉淀,F是Cu(OH)2,G+Ba(NO3)2→H,H为不溶于稀硝酸的白色沉淀,则H是BaSO4,E是CuSO4。I和X为常见的金属单质,J为浅绿色溶液,则x是Fe,I是Cu,J是FeSO4 。(1)物质H是BaSO4 。(2)B+Na2CO3→C+D的化学方程式为:Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH
(3)D+E→F+G的化学方程式为:2NaOH + CuSO4 = Cu(OH)2↓+ Na2SO4,由两种化合物互相交换成分生成另外两种化合物的反应是复分解反应。

 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案【题目】小明拿起家中的水壶准备煮水时,发现壶内有些褐色的固体。为了探究其成分,与兴趣小组同学查阅资料后获知这些褐色的固体是水垢,它可能是因为水中含有Ca(HCO3)2和Mg(HCO3)2等可溶性物质在加热时生成了CaCO3和Mg(OH)2。
(1)含有较多Ca(HCO3)2的水称_____(填“硬水”或“软水”),加热时发生反应的化学方程式为__________。
(2)小明认为本市属喀斯特地貌,以石灰岩为主,该水垢的成分只有CaCO3;但小白不同意,认为也可能只有Mg(OH)2,还可能______________。
(3)小明为了证明自己的猜想,设计如下实验方案:
实验操作 | 现 象 | 结 论 |
①取少量水垢于试管中,加入过量的_______。 | 观察到现象_________, 反应的化学方程式__________。 | 水垢中有CaCO3 |
②向①反应后的试管中滴加2-3滴NaOH溶液 | 观察到现象__________。 | 水垢中没有Mg(OH)2, 我的猜想成立 |
(4)小白不认可小明的结论,认为他的实验操作有缺陷,原因是_________________________。