��Ŀ����
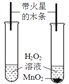
����Ŀ���ס��ҡ������ֹ��壨�������ᾧˮ�����ܽ��������ͼһ��ʾ����ش�
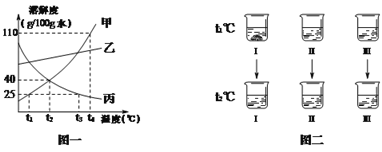
�� t1��ʱ��������ܽ����______g/100gˮ��
�� t2��ʱ���������ʵı�����Һ���������������Ĵ�С��ϵ��______��
�۹�����к��������ң�Ϊ�õ��ϴ����Ĺ���ף����õĽᾧ������______��
��t��ʱ��8 g���������20gˮ����ȫ�ܽ⣬t�����ȡֵ��Χ��______ ��
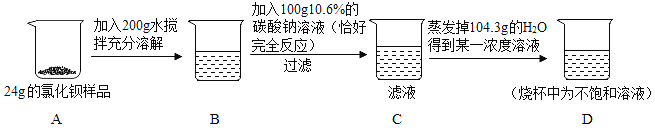
����ͼ����ʾ��t1��ʱ���ס��ҡ������ֹ����a g�ֱ����ʢ��100 gˮ���ձ��У�����ܽ��ֻ���ձ������й���ʣ�࣬������t2��ʱ�������ձ��о����塣���з�����ȷ����______��
A���ձ����з���Ĺ�������Ϊ�ס��ҡ���
B��t1��ʱ���ձ����е���Һ���Dz�������Һ
C��t2��ʱ�������ձ��е���Һ���Dz�������Һ
D��������t3��ʱ����һ���ձ��г��־���
���𰸡� 25 ��=������ ���½ᾧ t��t2��2�֣� BD
�������������ܽ�����߷�����𡣢����ܽ�����߿�֪��������ܽ����25g/100gˮ�������ܽ�����߿�֪��t2��ʱ���������ʵ��ܽ�ȴ�С��ϵ���ң���=������t2��ʱ���������ʵı�����Һ���������������Ĵ�С��ϵ���ң���=���������ܽ�����߿�֪���ס��ҵ��ܽ�ȶ����¶ȵ����߶������Ҽ����¶ȵ�Ӱ��仯�ϴʹ�����к��������ң�Ϊ�õ��ϴ����Ĺ���ף����õĽᾧ�����ǽ��½ᾧ����![]() ����t��ʱ��8 g���������20gˮ����ȫ�ܽ⣬t�����ȡֵ��Χ��t��t2����A��t1��ʱ�ס��ҡ������ֹ�����ܽ�ȴ�С��ϵ����=�����������ס��ҡ������ֹ����a g�ֱ����ʢ��100 gˮ���ձ��У�����ܽ��ֻ���ձ������й���ʣ�࣬������t2��ʱ�������ձ��о����塣˵���ձ����з���Ĺ����Ǽ����ձ����з���Ĺ������ж���������B�����ܽ�����߿�֪��t1��ʱ�ҡ������ܽ�ȱ�t2��ʱ���ܽ�ȴ��ס��ҡ������ֹ����a g�ֱ����ʢ��100 gˮ���ձ��У�����ܽ��ֻ���ձ������й���ʣ�࣬������t2��ʱ�������ձ��о����塣��t1��ʱ���ձ����DZ�����Һ���ձ����е���Һ���Dz�������Һ����ȷ��C��t2��ʱ���ҵ���Һ�Dz�������Һ������������ǡ���DZ�����Һ��������D�����ܽ�����߿�֪��t3��ʱ�����ܽ����t1��ʱ���ܽ�����Ϊ25g��t1��ʱ�����δȫ���ܽ�����������t3��ʱ�������ܽ�Ƚ������о�����������ȷ����ѡBD��
����t��ʱ��8 g���������20gˮ����ȫ�ܽ⣬t�����ȡֵ��Χ��t��t2����A��t1��ʱ�ס��ҡ������ֹ�����ܽ�ȴ�С��ϵ����=�����������ס��ҡ������ֹ����a g�ֱ����ʢ��100 gˮ���ձ��У�����ܽ��ֻ���ձ������й���ʣ�࣬������t2��ʱ�������ձ��о����塣˵���ձ����з���Ĺ����Ǽ����ձ����з���Ĺ������ж���������B�����ܽ�����߿�֪��t1��ʱ�ҡ������ܽ�ȱ�t2��ʱ���ܽ�ȴ��ס��ҡ������ֹ����a g�ֱ����ʢ��100 gˮ���ձ��У�����ܽ��ֻ���ձ������й���ʣ�࣬������t2��ʱ�������ձ��о����塣��t1��ʱ���ձ����DZ�����Һ���ձ����е���Һ���Dz�������Һ����ȷ��C��t2��ʱ���ҵ���Һ�Dz�������Һ������������ǡ���DZ�����Һ��������D�����ܽ�����߿�֪��t3��ʱ�����ܽ����t1��ʱ���ܽ�����Ϊ25g��t1��ʱ�����δȫ���ܽ�����������t3��ʱ�������ܽ�Ƚ������о�����������ȷ����ѡBD��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ����ƶԱ�ʵ�飬���Ʊ�����ѧϰ��ѧ����Ҫ���������жԱ�ʵ�������ﵽĿ�ĵ���
��� | A | B | C | D |
ʵ�� ��� |
|
|
|
|
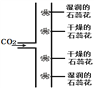
ʵ�� Ŀ�� | ̽��ͬ�������ڲ�ͬ�ܼ��е��ܽ��� | ̽��������ȼ�յ�����֮һ | ̽���������̵Ĵ����� | ̽��CO2���ܶȺ�ʯ�ﻨ����ԭ�� |
A. A B. B C. C D. D
����Ŀ��ijͬѧ������������Һ���뵽һ������ϡ�Ȼ�ͭ��Һ�У���������ɫ������ˮ�Ĺ��塣��ͬѧ����������ɫ��������ɫ�������������ɻ�
������������
(1)CuCl2��Һ��NaOH��Һ��Ӧ��������ɫ���塾Cu(OH)2�������������ƽ��ٵ�����»���������ɫ��ʽ�Ȼ�ͭ��Cux(OH)yClz�����䲻����ˮ�������ᷴӦ��
(2)Cu(OH) 2��60�濪ʼ�ֽ��������������100��ֽ���ȫ����ʽ�Ȼ�ͭ��300�濪ʼ�ֽ���������ͭ��ˮ���Ȼ��⣬��400��ֽ���ȫ��
���²⡿����ɫ��������ǣ���Cu(OH)2����Cux(OH)yClz���壻��___________��
����ٵ������ǣ�______________(�û�ѧ����ʽ��ʾ)��
��ʵ�顿��ͬѧȡ31.25g����ɫ���壬������100����ֺ�ɫ���塣����� _______
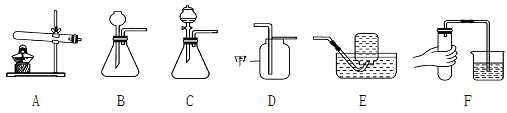
����ȷ���������ȵ�400�����������ٸı䣬��ʹ����������ȫ������ͨ����ͼ______(ѡ����������������)װ��(װ����ҩƷ����)��

ʵ�����ݣ������յõ�ʣ�����24.00g��
������������Һ��Ӧ�õ��ij��������ˡ�ϴ�Ӻ͵��º�ɣ��õ�����14.35g��
��Ũ����װ�����������±���
����ǰ | 100�� | 400�� |
250.00g | 251.80g | 253.60g |
���ۣ�����۳��������ʽ�Ȼ�ͭ��X��Y= _______��
��������
(1)��ʽ�Ȼ�ͭ����Ϊ�������ϵ����Ӽ�����ü�ʽ�Ȼ�ͭ��θҺ������Ӧ�Ļ�ѧ����ʽΪ___________________��
(2)Ϊʹʵ����������ɫ���壬�ٳ�������ɫ���壬Ӧ��______�Ľ�(ѡ�����)��
a��ʵ���н��Ȼ�ͭ��Һ�μӵ�����������Һ��
b��ʵ����Ӧ�ṩ��������Ũ������������Һ
c��ʵ��Ӧ����80���ˮԡ�н���